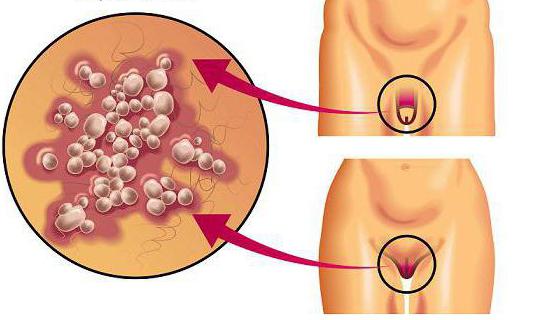
Днк вируса простого герпеса 1 и 2 типа в крови

Вирус простого герпеса (ВПГ) – ДНК–содержащий вирус Herpes simplex virus семейства Herpesviridae подсемейства Alphaherpesvirinae. Согласно статистическим данным ВОЗ, инфекции, обусловленные ВПГ, занимают второе место по распространенности среди вирусных заболеваний человека. Различают два серотипа ВПГ – ВПГ-1 и ВПГ-2. Оба типа вируса вызывают инфекционные заболевания человека различной степени тяжести от характерных везикулезных или пустулезных высыпаний на коже и слизистых до поражений ЦНС. ВПГ-1 – причина офтальмогерпеса, протекающего в форме кератита или кератоиридоциклита, реже увеита, в единичных случаях — ретинита, блефароконъюнктивита. Заболевание может привести к помутнению роговицы и вторичной глаукоме. ВПГ-1 — основная причина энцефалита у взрослого населения стран умеренного климата, при этом только у 6–10% больных отмечается одновременное поражение кожи.
В ходе проведения эпидемиологических исследований установлено наличие специфических АТ к ВПГ у 90–95% обследуемых лиц среди взрослого населения, при этом первичная инфекция манифестно протекает лишь у 20–30% инфицированных.
ВПГ характеризуется коротким циклом репродукции в клеточных культурах и оказывает сильное цитопатическое действие. Он способен к репродукции в различных типах клеток, чаще персистирует в ЦНС, преимущественно в ганглиях, поддерживая латентную инфекцию с возможностью периодической реактивации. Наиболее часто вызывает кожно-слизистые формы заболевания, а также поражение ЦНС и глаз. Геном ВПГможет интегрироваться с генами других вирусов (включая ВИЧ), вызывая их активацию, также возможен его переход в активное состояние на фоне развития иных вирусных и бактериальных инфекций.
Пути передачи ВПГ: воздушно-капельный, половой, контактно-бытовой, вертикальный, парентеральный. Факторами передачи ВПГ служат кровь, слюна, моча, везикулярный и вагинальный секрет, сперма. Входными воротами являются поврежденные слизистые оболочки и кожа. По периферическим нервам вирус доходит до ганглиев, где сохраняется пожизненно. При активации ВПГ распространяется по нерву к первоначальному очагу поражения (механизм “замкнутого цикла” – циклическая миграция вируса между ганглием и поверхностью кожи). Может происходить лимфогенная и гематогенная диссеминация возбудителя, что особенно характерно для недоношенных новорожденных и лиц с выраженным иммунодефицитом (в т. ч. при ВИЧ-инфекции). ВПГ обнаруживается на лимфоцитах, эритроцитах, тромбоцитах, при проникновении вируса в ткани и органы возможно их повреждение вследствие его цитопатического действия. Сохраняющиеся в течение всей жизни у человека вируснейтрализующие АТ (даже в высоких титрах), хотя и препятствуют распространению инфекции, но не предупреждают рецидивов.
Выделение ВПГ продолжается значительное время при первичном инфицировании (ДНК выявляется в плазме крови в течение 4–6 недель), при рецидивах – не более 10 дней. Формирование противогерпетического иммунитета происходит как при манифестном, так и при бессимптомном течении инфекции. При первом контакте АГ с клетками иммунной системы в течение 14–28 дней формируется первичный иммунный ответ, который у иммунокомпетентных лиц проявляется образованием интерферонов, выработкой специфических АТ (вначале – IgM, впоследствии – IgA и IgG), повышением активности естественных киллеров – NK-клеток и формированием мощного пула высокоспециализированных киллеров. В случае реактивации или реинфекции возникает повторный контакт клеток иммунной системы с АГ, образуются АТ и Т-киллеры. Реактивация сопровождается продукцией АТ IgM (редко даже при наличии типичных высыпаний), АТ IgА (чаще) и IgG.
ВПГ (преимущественно ВПГ-2) вызывает генитальный герпес – хроническое рецидивирующее заболевание. Клинические проявления первичного эпизода инфекции, вызванной разными типами вируса сходны, однако инфекции, вызванной ВПГ-2, в гораздо большей степени свойственен рецидивирующий характер. Передача вируса происходит при половых контактах, очаг инфекции локализуется на слизистой и коже половых органов и перигенитальной зоны. Размножение вируса в клетках эпителия приводит к образованию очага сгруппированных пузырьков (папул, везикул), в которых содержатся вирусные частицы, сопровождается покраснением, зудом. Первичный эпизод протекает острее (обычно с симптомами интоксикации), чем последующие рецидивы. Часто возникают симптомы дизурии, признаки эрозии шейки матки.
На ранних стадиях ВИЧ-инфекции течение заболеваний, вызванных ВПГ-1 или ВПГ-2, короткое и типичное. Частым признаком углубления иммуносупрессии и перехода латентной стадии ВИЧ-инфекции в стадию вторичных заболеваний служит развитие опоясывающего лишая. Наличие стойких глубоких вирусных поражений кожи, повторный или диссеминированный опоясывающий лишай, локализованная саркома Капоши — одни из клинических критериев стадии вторичных заболеваний ВИЧ-инфекции. У больных с количеством CD4+-клеток менее 50 клеток/мкл отсутствует тенденция к самостоятельному заживлению эрозивно-язвенных дефектов. Частота герпетического энцефалита среди поражений ЦНС при ВИЧ-инфекции — около 1–3%. У больных СПИДом с наличием глубокого иммунодефицита заболевание нередко протекает атипично: болезнь начинается подостро и медленно прогрессирует до тяжелейших проявлений энцефалита.
Герпетическая инфекция даже при бессимптомном течении способна вызвать целый ряд патологий у беременной и новорожденного. Наибольшую угрозу репродуктивной функции представляет генитальный герпес, который в 80% случаев обусловлен ВПГ-2 и в 20% – ВПГ-1. Бессимптомное течение чаще имеет место у женщин и более типично для ВПГ-2, чем для ВПГ-1. Первичное инфицирование или рецидивы во время беременности наиболее опасны для плода, поскольку могут привести к самопроизвольному выкидышу, гибели плода, мертворождению, порокам развития. Заражение плода и новорожденного чаще отмечается при бессимптомном течении генитального герпеса, чем при клинически выраженном типичном течении. Новорожденный может приобрести герпетическую инфекцию внутриутробно, во время родов (в 75–80% случаев), либо постнатально.
ВПГ-2 может проникать в полость матки через цервикальный канал с поражением плода в 20–30% случаев; трансплацентарное инфицирование может происходить в 5–20% случаев, инфицирование во время родов – в 40% случаев. Возможна передача вируса при выполнении медицинских процедур. При типичных клинических проявлениях диагноз герпетической инфекции трудностей не представляет, тогда как при атипичных формах верифицируется на основании результатов лабораторных исследований, при этом приоритетными должны быть исследования, направленные на выявление маркеров текущей (активной) инфекции. Активация инфекционного процесса при герпетической инфекции, даже при наличии клинических проявлений в стадии обострения, редко сопровождается выработкой АТ-ВПГ IgM (чаще – при первичной инфекции либо реинфекции), как правило, при этом отмечают появление АТ-ВПГ IgА.
Целесообразными являются диагностические исследования для обнаружения ВПГ или его маркеров при наличии в анамнезе пациента указаний на рецидивирующую инфекцию либо на дебют герпетической инфекции в период беременности.
Дифференциальная диагностика. При наличии инфекционного синдрома (длительный субфебрилитет, лимфаденопатия, гепато- или гепатоспленомегалия) – токсоплазмоз, цитомегаловирусная инфекция и инфекция, вызванная ВЭБ; контактный дерматит, инфекционные заболевания, сопровождающиеся везикулезными высыпаниями на коже и слизистых оболочках (ветряная оспа, опоясывающий герпес, пиодермия и др.); эрозивно–язвенные поражения гениталий, обусловленные Treponema pallidum, Haemophilus ducreyi; болезнь Крона, синдром Бехчета, фиксированная токсикодермия, менингоэнцефалиты и менингиты неясной этиологии, увеиты и кератоконъюнктивиты неясной этиологии).
Показания к обследованию
- Планирование беременности;
- женщины, имеющие в анамнезе либо на момент обращения типичные герпетические высыпания любой локализации, в т. ч. рецидивирующий генитальный герпес, или наличие пузырьковых и/или эрозивных высыпаний на коже, ягодицах, бедрах, слизисто–гнойные выделения из влагалища;
- наличие полового контакта с партнером, имеющим генитальный герпес;
- атипичная форма заболевания: отсутствие зуда или жжения, отсутствие везикул, веррукозные узелки; обширные кожные поражения (до 10% случаев предполагаемого опоясывающего герпеса обусловлено не ВЗВ, а ВПГ);
- женщины с отягощенным акушерским анамнезом (перинатальные потери, рождение ребенка с врожденными пороками развития);
- беременные женщины (в первую очередь имеющие УЗИ-признаки внутриутробной инфекции, лимфоаденопатии, лихорадку, гепатит и гепатоспленомегалию неясного генеза);
- дети с признаками внутриутробной инфекции, врожденными пороками развития или наличием на коже или слизистых оболочках везикул или корочек;
- дети, рожденные от матерей, перенесших генитальный герпес во время беременности;
- ациенты (в первую очередь новорожденные) с сепсисом, гепатитами, менингоэнцефалитом, пневмонией, поражением глаз (увеит, кератит, ретинит, ретинальный некроз), поражением ЖКТ.
Материал для исследования
- Содержимое пузырьков/везикул со слизистых оболочек и кожи половых органов мужчин и женщин – микроскопические исследования, культуральные исследования, выявление АГ, выявление ДНК;
- мазки (соскобы) со слизистых оболочек цервикального канала, уретры (при отсутствии видимых пузырьковых высыпаний или эрозивно-язвенных поражений) – выявление ДНК;
- сыворотка крови, СМЖ (по показаниям) – выявление АТ.
Этиологическая лабораторная диагностика включает микроскопическое исследование, выделение и идентификация вируса в культуре клеток, выявление АГ или ДНК возбудителя, определение специфических АТ.
Сравнительная характеристика методов лабораторной диагностики (вирус простого герпеса — анализ). Среди методов лабораторной диагностики “золотым стандартом” долгое время считали выделение ВПГ в культуре клеток из крови, СМЖ, содержимого везикулезных или пустулезных высыпаний и других локусов (носоглотки, конъюнктивы, уретры, влагалища, цервикального канала). Данный метод предполагает изоляцию вируса при заражении биологическим материалом чувствительных культур клеток с его последующей идентификацией. К неоспоримым преимуществам метода относятся: возможность определения активности инфекции при наличии клинических проявлений и проведения типирования вируса, а также установления чувствительности к противовирусным препаратам. Однако длительность анализа (1–8 дней), трудоемкость, высокая стоимость и необходимость определенных условий проведения исследований затрудняет применение данного метода для рутинной лабораторной диагностики заболевания. Чувствительность достигает 70–80%, специфичность – 100%.
Материал с поверхности высыпаний может быть использован для микроскопических (окраска препаратов по Романовскому–Гимзе) или цитологических (окраска препаратов по Тцанку и Папаниколау) исследований. Названные процедуры имеют низкую диагностическую специфичность (не позволяют дифференцировать ВПГ от других герпес-вирусов) и чувствительность (не более 60%), поэтому не могут считаться надежными методами диагностики.
Выявление АГ ВПГ в крови, СМЖ, содержимом везикулезных или пустулезных высыпаний и других локусов (носоглотки, конъюнктивы, уретры, влагалища, цервикального канала) проводят методами РИФ и РНИФ с использованием моноклональных или высокоочищенных поликлональных АТ. При использовании метода ИФА чувствительность исследования возрастает до 95% и более, специфичность при манифестном герпесе варьирует от 62 до 100%. Однако большинство наборов реагентов для выявления антигена ВПГ методом ИФА не позволяют провести дифференцирование серотипов вируса.
Обнаружение ДНК ВПГ-1 и/или ВПГ-2 при использовании ПЦР в различном биологическом материале превосходит чувствительность обнаружения ВПГ при использовании вирусологического исследования. Выявление ВПГ в соскобах со слизистых оболочек полости рта, урогенитального тракта, в отделяемом пузырьковых высыпаний (везикул) и эрозивно–язвенных поражений кожи с помощью ПЦР является методом выбора. Несомненную ценность имеет определение количества ДНК ВПГ методом ПЦР в режиме реального времени, результаты исследования можно использовать как с диагностической целью, так и для оценки эффективности лечения.
Для выявления АТ к ВПГ разных классов IgА, IgG, IgM, суммарных к антигенам ВПГ обоих типов или типоспецифичных, применяют методы РНИФ или ИФА, для определения авидности АТ IgG – метод ИФА. Наибольшее диагностическое значение имеет детекция АТ IgM как показателя активности процесса, их выявление может свидетельствовать об остром заболевании, реинфекции, суперинфекции или реактивации. Однако в клинически выраженных случаях, в т. ч. при типичном течении генитального или неонатального герпеса, специфические АТ IgM выявляются редко (в 3–6% случаев). Определение авидности АТ-ВПГ IgG несет низкую информационную нагрузку: реактивация при клинически выраженных случаях сопровождалась наличием высокоавидных АТ. Тест на выявление АТ-ВПГ IgА является методом выбора наряду с определением ДНК либо АГ ВПГ при определении активности инфекционного процесса.
Показания к применению различных лабораторных исследований. Определение АТ целесообразно проводить для подтверждения первичной инфекции, а также установления диагноза у пациентов с бессимптомным и атипичным течением заболевания.
У беременных женщин (скрининг) целесообразно проведение исследований для выявления АТ-ВПГ IgМ, а также выявление АТ-ВПГ IgА. Для беременных высокого инфекционного риска дополнительно рекомендуется определение ДНК и АГ ВПГ в лейкоцитарной взвеси или в материале из предполагаемого очага.
При подозрении на внутриутробную инфекцию рекомендуется выявление ДНК вируса в пуповинной крови, у новорожденных – детекция ДНК вируса в различных биологических пробах (отделяемое пузырьковых высыпаний (везикул) эрозивно– язвенных поражений кожи и слизистых оболочек, ротоглотки, конъюнктивы; периферическая кровь, СМЖ, моча и др.), а также определение АТ-ВПГ IgМ и IgА в крови. Учитывая высокую диагностическую значимость определения ДНК вируса методом ПЦР и наличие зависимости между летальностью у новорожденных и виремией, вызванной ВПГ, некоторые исследователи рекомендуют использовать этот метод для лабораторного скрининга генерализованной герпетической инфекции детей, относящихся к группе высокого риска.
Выявление АГ-ВПГ в различных биологических пробах предлагается применять в качестве экспресс-тестов для дифференцирования типов вируса при скрининге популяций с высоким уровнем заболеваемости, а также при мониторинге заболевания.
У больных ВИЧ-инфекцией с атипичными клиническими проявлениями кожных поражений в диагностике отдается предпочтение выявлению ДНК ВПГ методом ПЦР как самому чувствительному методу лабораторной диагностики.
Особенности интерпретации результатов. Обнаружение вирусоспецифических АТ IgM может свидетельствовать о первичной инфекции, реже – о реактивации или реинфекции, выявление АТ-ВПГ IgА – об активности инфекционного процесса (затяжное течение при дебюте герпетической инфекции, реинфекции или реактивации). О врожденной инфекции (неонатальный герпес) свидетельствует присутствие АТ-ВПГ IgM и(или) IgА. Выявление АТ IgG отражает латентную инфекцию (инфицирование).
Выявление ДНК ВПГ свидетельствует о наличии активной (репликативной) стадии вирусной инфекции с учетом выраженности клинических проявлений. Выявление ДНК ВПГ-1 и/или ВПГ-2 методом ПЦР позволяет при однократном тестировании установить факт внутриутробного инфицирования плода; при проведении обследования в первые 24–48 ч после рождения лабораторно подтвердить врожденную инфекцию, вызванную ВПГ.
Диагностическое значение (специфичность и чувствительность) обнаружения ДНК ВПГ в СМЖ у больных ВИЧ-инфекцией с поражением ЦНС окончательно не установлены. Возможно, для подтверждения герпетической этиологии энцефалита необходимо определение концентрации ДНК ВПГ в СМЖ. Исследование для обнаружения ДНК ВПГ в крови малоинформативно в связи кратковременным нахождением ВПГ в сосудистом русле, следовательно, возможно получение отрицательного результата несмотря на развитие клинически выраженного заболевания.
Источник
Герпес — это одно из наиболее распространенных вирусных заболеваний на планете. По данным статистики, не менее 90% населения является носителями этого вируса. Клинические признаки отличаются при разных типах герпеса, болезнь может проявляться на коже и слизистых оболочках. Анализ крови на герпес 1 и 2 типа и расшифровка данных — это способ выявить возбудителя, определить его тип и выбрать подходящую схему лечения.

Что представляет собой возбудитель?
Возбудитель герпеса — это ДНК-содержащий вирус. Чаще всего он поражает кожу лица, слизистые оболочки глаз, половых органов, реже — ткани нервной системы и внутренние органы.
Заражение может происходить одним из следующих способов:
- контактным (в том числе при использовании общих предметов быта и личной гигиены);
- воздушно-капельным;
- половым;
- вертикальным (от матери к ребенку при беременности и в процессе родов).
После проникновения в организм вирус может не проявляться клинически в течение длительного времени. Иммунная система человека держит популяцию возбудителя под контролем, и он не способен размножаться. Первые симптомы возникают при снижении уровня иммунной защиты, в том числе при сезонных иммунодефицитах. Поэтому герпес часто сопровождает другие вирусные и бактериальные заболевания, грибковые инфекции.
Больной может не знать, что является вирусоносителем, но при этом заражать окружающих.

Герпесвирус 1 типа
Вирус простого герпеса первого типа — это самый распространенный возбудитель. Он проникает в организм человека еще в детском возрасте и дает периодические рецидивы.
Чаще всего болезнь локализуется на коже лица и тела и проявляется следующими симптомами:
- покраснение кожи в месте активизации вируса;
- появление мелкой сыпи (пузырьки вскрываются самостоятельно, а на их месте образуются язвы);
- зуд и отечность.
Заболевание проявляется локально, но некоторые пациенты жалуются также на повышение температуры, озноб, слабость и мышечную боль. В период рецидива герпеса больной максимально опасен для окружающих, так как возбудитель находится в содержимом пузырьков.
Герпесвирус 2 типа
Герпес второго типа относят к заболеваниям, передающимся половым путем. Кроме того, существуют еще контактный, бытовой и вертикальный пути передачи. Клинически болезнь проявляется сыпью на половых органах и коже бедер. Исследования на герпесвирус обязательны при беременности. Вирус опасен для плода: существует риск развития патологий, а также инфицирования младенца во время родов.
В каких случаях нужно обращаться в лабораторию?

Во время рецидива болезни вирус герпеса 1 и 2 типа можно определить путем простого осмотра. Характерная зудящая сыпь, которая имеет определенную локализацию, — это единственный признак, который будет являться основанием для постановки диагноза. Кроме того, пузырьки часто появляются на одном и том же месте, с одинаковой стороны.
Сдавать кровь в лабораторию для анализа нужно только в нескольких случаях:
- если герпес проявляется нестандартно, в стертой форме или с осложнениями;
- во время планирования беременности;
- если нужно выяснить срок заражения (например, при беременности для оценки потенциального риска для плода).
Сыпь может служить признаком большого количества заболеваний инфекционного и незаразного происхождения. По данным анализа крови можно определить тип вируса, убедиться в диагнозе и назначить лечение по необходимости.
Методы определения вируса герпеса в крови

Существует несколько методик обнаружения герпесвируса в крови. Они эффективны при спорных ситуациях, а также в тех случаях, если болезнь протекает бессимптомно. Во время рецидива можно также исследовать содержимое пузырьков, соскобы кожи или мазки слизистых оболочек. Лечащий врач определит, какие анализы нужно сдать, исходя из возможностей лаборатории и финансового положения пациента.
Существует несколько стандартных правил, которые позволят получить наиболее точный результат. Анализы сдают на голодный желудок. Чаще всего кровь собирают утром, с 8 до 10 часов. Накануне не стоит употреблять жирную пищу и алкоголь. Также на результат анализов могут повлиять стрессы или любое другое эмоциональное перенапряжение.
Анализ на герпес 1 и 2 типа чаще всего проводят двумя методами — ПЦР (полимеразная цепная реакция) и ИФА (иммуноферментный анализ). Также могут использоваться другие способы, в зависимости от оснащения лаборатории и ее технических возможностей.
Полимеразная цепная реакция (ПЦР)
ПЦР — это чувствительная реакция, которая позволяет обнаружить в исследуемом материале ДНК вирусных клеток. Суть метода сводится к тому, что определенный ген многократно копируют, в результате чего можно выявить наличие и тип возбудителя. Важно, что реакция не произойдет, если исследуемой ДНК в материале нет.
Полимеразная цепная реакция позволяет обнаружить вирус непосредственно после заражения, задолго до того, как болезнь начнет проявляться клинически. Также ее назначают в тех случаях, когда нужно определить конкретный тип вируса, а не просто его наличие.
Лаборатория предоставляет бланки с показателями, которые легко расшифровать самостоятельно. Положительный результат свидетельствует о присутствии вируса в крови, отрицательный — об отсутствии. Это наиболее достоверный и чувствительный анализ, который выявляет даже самую малую концентрацию возбудителя. Полимеразная цепная реакция дает один из наиболее достоверных результатов, поэтому считается дорогостоящей. Также в бланках содержится информация о типе герпеса.
Иммуноферментный анализ (ИФА)

ИФА — это реакция, которая основана на выделении комплекса антиген—антитело. Вирус герпеса 1 или 2 типа— это антиген для организма (чужеродное вещество), в ответ на который иммунная система выделяет специальные белки — антитела (иммуноглобулины или Ig).
Антитела переносятся в током крови по организму в очаг заболевания и там начинают бороться с инфекцией. Существует несколько основных классов иммуноглобулинов, которые можно обнаружить по время анализа на герпес:
- IgM — это первые антитела, которые формируются в организме больного. В крови пациента их можно найти в течение 2-х недель с момента инфицирования. Кроме того, эти белки появляются в период пробуждения вируса при хроническом герпесе.
- IgG — это антитела, на основании которых можно говорить о хронической инфекции, которая находится в организме больного уже в течение длительного времени. Количество иммуноглобулинов этого класса резко возрастает при очередном рецидиве герпеса.
- IgG к предранним белкам вируса герпеса — это белки-антитела, которые возникают в крови вслед за IgM и также указывают на наличие заболевания в острой или хронической форме.
- Оценивают и такой показатель, как авидность IgG. Он характеризует способность этого иммуноглобулина связываться с вирусом и образовывать комплекс антиген—антитело. В начале болезни этот показатель слабо выражен, но в активную фазу заболевания резко возрастает.
Расшифровку результатов проводит врач. В каждой лаборатории существуют собственные показатели нормы. Больной получает бланк, в котором указаны его значения антител, а также те, от которых необходимо отталкиваться. Если количество иммуноглобулинов ниже нормы — результат отрицательный, если выше — положительный.
Далее необходимо сопоставить концентрацию разных классов антител в крови и расшифровать данные по таблице:
| IgM | IgG к предранним белкам | Поздние IgG | Результат |
| — | + | + | Если ранее пациент не болел герпесом, такой результат говорит о первичной острой инфекции. При беременности в таком случае существует угроза для плода. Если человек — носитель вируса (болезнь ранее проявлялась клинически или обнаруживалась лабораторным способом), речь идет о рецидиве герпеса. Иммунная система матери при беременности обеспечивает защиту плоду, но может быть необходимо ее лечение. |
| — | — | + | Пациент является носителем вируса простого герпеса, и в его организме выработан иммунитет, который не позволяет болезни проявляться клинически. Такой результат обнаруживают в периоды ремиссии герпеса. |
| + | + | — | Такие данные говорят о первой стадии развития герпесной инфекции. В эту фазу существует угроза для жизни плода. |
| + | + | + | |
| — | — | — | Человек никогда не сталкивался с вирусом герпеса, и его иммунная система не предоставляет защиту от него. Если этот анализ проводится во время беременности, врачи беспокоятся о занесении инфекции и развития острого герпеса. В таком случае состояние плода будет находиться под угрозой. |
Отдельно проводится расшифровка анализов на авидность IgG. Возможные результаты представлены в таблице:
| Индекс авидности, % | Результат |
| 50—60% | Этот показатель является пороговой зоной и не может говорить о каком-либо результате. Исследования необходимо повторить через 14 дней. |
| Ниже 50% | Результат говорит о наличии низкоавидных иммуноглобулинов. Они обнаруживаются при первичной инфекции. |
| Выше 60 % | Выявлены высокоавидные иммуноглобулины. Такой результат может появляться при хроническом герпесе или у носителей вируса. |
| Отрицательно | Организм пациента никогда не контактировал с вирусом. При беременности необходимо следить за показателями, поскольку иммунная защита как матери, так и плода, отсутствует. |
Результаты анализов могут отличаться в разных лабораториях. Они зависят от оборудования и других факторов, но, в основном, бывают достоверными.
Реакция иммунофлюоресценции (РИФ)
 РИФ — это еще один способ обнаружить вирус в исследуемом материале, в том числе в крови. Эта реакция показывает наиболее точный результат, если концентрация возбудителя высока. Суть метода сводится к добавлению в субстрат (кровь) специальных красителей с антителами и его последующей микроскопии. Если вирус присутствует, он вступает в химические реакции с антителами и светится под микроскопом.
РИФ — это еще один способ обнаружить вирус в исследуемом материале, в том числе в крови. Эта реакция показывает наиболее точный результат, если концентрация возбудителя высока. Суть метода сводится к добавлению в субстрат (кровь) специальных красителей с антителами и его последующей микроскопии. Если вирус присутствует, он вступает в химические реакции с антителами и светится под микроскопом.
Расшифровка анализа крови на герпес путем РИФ — это результаты микроскопии. Характерное свечение говорит о наличии возбудителя. На точность данных повлияет не только количество вируса герпеса, но и наличие другой инфекции в крови. Если она там находится в высокой концентрации, можно получить ложноположительный результат.
Культуральный метод
Этот метод заключается в выделении вируса из исследуемого материала и заражении биологических объектов (культуры клеток, куриных эмбрионов) в лабораторных условиях. Способ требует больших затрат времени и не используется в обычных ситуациях. Чаще всего его применяют для научных исследований. Для его выполнения необходима специально оборудованная вирусологическая лаборатория для изоляции возбудителя в помещении и предотвращения его распространения.

Заключение
Герпес — это одно из наиболее распространенных заболеваний в мире. Его характерная особенность заключается в том, что возбудитель остается в крови пациента в течение многих лет и только иногда вызывает клинические проявления болезни. Он не представляет опасности для взрослого человека, но может спровоцировать патологии беременности и передаваться от матери к ребенку при родах. Лучший способ профилактики герпеса — поддержка собственной иммунной системы, которая будет контролировать популяцию вируса и предотвратит появление симптомов болезни.
Источник