Галавит кому назначали от герпеса
Средняя цена: 507-914 руб.
Латинское название: Galavit
Код ATX: L03 Иммуностимуляторы
Действующее вещество: аминодигидрофталазиндион натрия (Галавит®)
Производитель: ООО «Сэлвим». 123290, Россия, Москва, туп. Магистральный 1-й, 5А, ком. 91.
При беременности: Использовать с осторожностью
Прием детьми: Использовать с осторожностью
Инструкция
Галавит при герпесе – эффективный препарат, оказывающий иммуномодулирующее и противовоспалительное действие. Эти ректальные свечи используют для лечения генитального герпеса. С их помощью удается не только избавиться от болезненных и дискомфортных ощущений, но и укрепить иммунитет.
Показания к применению
Суппозитории Галавит показаны при лечении заболеваний, вызванных вирусами простого герпеса 2 типа, в результате которых поражаются половые органы. Используются в комплексной терапии с противовирусными препаратами.
Как лечить вагинальный герпес? Подробнее тут.
Способ применения и дозы
Перед введением свечей необходимо опорожнить кишечник. Рекомендуемая доза при обострении герпеса у взрослых и детей старше 12 лет составляет 100 мг в сутки. Курс лечения при острой форме герпеса предполагает применение 20-25 суппозиториев. Первые 10 дней нужно ежедневно вводить по 1 свече, после чего дозу уменьшают до 100 мг (1 раз в 2 дня). При хронической форме герпеса первые 5 дней вводят по 1 свече, после чего на протяжении 1,5 месяца необходимо вводить 100 мг Галавита каждые 2 суток.
Побочные действия
Препарат переносится пациентами хорошо. В редких случаях возникает аллергическая реакция, проявляющаяся в виде зуда, сыпи или удушья. Если появляются дискомфортные ощущения, нужно прекратить использование медикамента и обратиться за медицинской помощью.
Галавит не оказывает влияния на управление транспортным средством.
Противопоказания
Противопоказаниями к использованию суппозиториев являются:
- непереносимость компонентов препарата;
- беременность и лактация;
- возраст до 12 лет.
Длительность лечения
Продолжительность терапии генитального герпеса свечами Галавит определяется лечащим врачом, который учитывает возраст, степень тяжести и симптомы заболевания, а также результаты анализов. Первая часть терапевтического курса длится от 7 до 10 дней, в течение которых лекарство вводится ежедневно. Затем интервал между приемами Галавита увеличивают. При тяжелой форме герпесвирусной инфекции весь курс лечения может продлиться до 3 месяцев.
Взаимодействие с другими препаратами
Суппозитории не оказывают негативного воздействия на организм пациента при комплексной терапии герпеса в сочетании с другими лекарственными препаратами. Тем не менее перед применением нужно обязательно проконсультироваться с врачом.
Рассматривая совместимость с алкоголем, следует учесть, что небольшие дозы спиртного (100-150 мл) не вызывают побочных симптомов, а в случае превышения этой дозировки человек может ощущать кратковременное головокружение, тошноту и жжение в анусе.
Передозировка
Случаи передозировки препаратом не зафиксированы, однако в результате чрезмерного употребления иммуномодулятора может нарушиться баланс микрофлоры.
Условия хранения
Хранить свечи следует при температуре +5…+12°C в месте, которое защищено от солнца и недоступно для детей.
Состав и форма выпуска
Галавит выпускается в виде ректальных свечей белого или желтоватого цвета (50 и 100 мг). Одна упаковка с ячейками содержит 5 суппозиториев.
Активным веществом препарата является аминодигидрофталазиндион натрия, который начинает действовать спустя 30-60 минут после применения свечей, а его эффективность сохраняется в течение 72 часов. Вспомогательным веществом Галавита является витепсол (гидрофобная основа).
Беременность и лактация
В 1 триместре беременности Галавит не рекомендуется использовать, т. к. при попадании компонентов лекарственного средства в системный кровоток они передаются плоду. Во 2 и 3 триместрах врач может назначить лечение препаратом, но лишь в том случае, если предполагаемая польза для матери превышает потенциальный риск для плода.
Ввиду отсутствия информации о действии Галавита на детский организм при грудном вскармливании от применения препарата следует отказаться.
Особенности лечения герпеса при беременности.
Применение в детском возрасте
При тяжелых формах поражения герпесом, если не помогают другие методы лечения, суппозитории назначают с 6 лет. Суточная доза детям младше 12 лет составляет 50 мг.
Условия отпуска из аптек
Без рецепта.
Оценка препарата:
(пока оценок нет)
Загрузка…
Источник
Комментарии
Опубликовано в журнале, Новые лекарства 2003, № 3 А. Е. Шульженко, И. Н. Зуйкова
НИИ иммунологии МЗРФ
Генитальный герпес (ГГ) в настоящее время относится к наиболее частым заболеваниям, передаваемым половым путем, и представляет собой одну из наиболее социально значимых проблем в медицине. Частота генитального герпеса, регистрирующаяся в разных странах, значительно увеличилась за последние годы, что во многом связано с распространением бессимптомной и недиагностированной герпетической инфекции.
По современным оценкам в России, число больных, обращающихся по поводу генитального герпеса, составляет около 15% от реальной частоты заболевания, а общее число больных, страдающих острыми и рецидивирующими формами ГГ, может составлять около 8 млн. человек. В целом у 90% взрослого населения в крови содержатся антитела к вирусам простого герпеса, при этом многие из них ни разу не переносили клинически выраженного эпизода заболевания.
В зависимости от биологических свойств и путей передачи вирусы простого герпеса (ВПГ) условно подразделяют на два типа: ВПГ первого типа (ВПГ 1) и ВПГ второго типа (ВПГ 2). В подавляющем большинстве случаев при генитальном герпесе инфекционным агентом является ВПГ 2, при этом в 10-26% случаев генитальный герпес вызван ВПГ 1, что объясняется орально-генитальным путем заражения. Заболевание передается как от больного генитальным герпесом, так и от носителей вируса, не имеющих (что особенно важно) клинических проявлений заболевания. Следует отметить, что наличие инфицированности ВПГ 1 не предотвращает возможности реинфицирования ВПГ 2, при этом вполне вероятно одновременное сосуществование нескольких видов и штаммов вирусов.
Входными воротами для генитального герпеса служат кожные покровы, слизистые оболочки половых органов. Далее вирус распространяется преимущественно по нервным окончаниям, а также по гематогенным и лимфогенным путям. Спектр клинических проявлений герпетической инфекции характеризуется значительным полиморфизмом вследствие тропизма ВПГ к эпителиальным и нервным тканям и зависит от места локализации патологического процесса, его интенсивности и распространенности, а также состояния иммунной системы.
Согласно данным исследователей только 20% инфицированных ВПГ имеют диагностированный генитальный герпес, 60% — нераспознанный симптоматический генитальный герпес (атипичную форму) и 20% — бессимптомный герпес. Бессимптомная форма представляет наибольшую эпидемиологическую угрозу, т. к. больные с бессимптомным генитальным герпесом чаще всего становятся источниками инфицирования, а беременные женщины — источником инфицирования ребенка.
Герпетическая инфекция, наряду с цитомегаловирусной, является одним из главных повреждающих факторов плода и новорожденного, вызывая увеличение самопроизвольных абортов, преждевременных родов, рождение детей с патологией ЦНС и внутренних органов. Кроме того, многочисленные исследования показали наличие связи между рецидивирующей герпесвирусной инфекцией и развитием онкологической патологии у женщин.
Исследования последних лет указывают на частое сочетание герпетической инфекции гениталий с хламидиями, микоплазмами, трихомонадами, гарднереллами, грибами рода Candida. Длительная персистенция герпесвирусов в организме человека и специфический иммунодефицит, сформированный у больных рецидивирующим генитальным герпесом, способствуют присоединению других инфекций урогенитального тракта.
Характерной особенностью герпесвирусов является способность, попав однажды, пожизненно персистировать в организме хозяина и вызывать многообразные формы заболеваний на фоне иммунной дисфункции. В латентной фазе экспрессируется ограниченное количество вирусных генов, продукты которых поддерживают вирус в неактивном состоянии. Реактивация, т. е. переход от персистенции к активной репликации, наблюдается при нарушении динамического равновесия между иммунным гомеостазом и вирусами, что отражает срыв контролирующих механизмов хозяина. Способность к длительному персистированию обусловливается наличием у герпесвирусов многочисленных механизмов, воздействующих на формирование противовирусной иммунной защиты и приводящих к уклонению патогенов от иммунологического надзора. Индуцированное вирусами ослабление иммунной защиты позволяет им благополучно размножаться и распространяться в организме хозяина в течение длительного времени.
Таким образом, в лечении рецидивирующего генитального герпеса до сих пор, несмотря на существенное развитие фармакологической терапии, имеются значительные методические и практические трудности. Современные фармакологические методы не способны прервать длительную персистенцию герпесвирусов в организме человека, а также бессимптомное вирусовыделение.
В тактике лечения генитального герпеса можно выделить следующие задачи:
- ослабление выраженности клинических симптомов инфекции (зуд, жжение, боль, лихорадка и лимфоаденопатия);
- сокращение срока полной реэпителизации поражения;
- уменьшение частоты и тяжести рецидивов;
- предупреждение передачи инфекции половому партнеру или новорожденному.
Для достижения этих задач в настоящее время используются следующие подходы: противовирусная химиотерапия, иммунотерапия и комбинация этих методов.
“Золотым стандартом” противогерпетической химиотерапии является первый лечебный синтетический нуклеозид — Ацикловир, ациклический аналог гуанозина. Гуанозин — один из самых частых концевых и внутренних нуклеозидов ДНК герпес-вирусов и составляет 16% всех повторов в цепях ДНК герпеса, что обусловило очень высокую терапевтическую активность Ацикловира. Механизм действия Ацикловира основан на его высокоспецифичности в отношении вирусной тимидинкиназы, которая фосфорилирует Ацикловир. ДНК-полимераза вируса ошибочно включает фосфорилированный Ацикловир вместо естественного дезоксигуанозинтрифосфата в концевые участки новых вирусных ДНК. Это обрывает процесс репликации вируса на любой стадии, и новые генерации вирусов не образуются.
В последнее время синтезированы и широко используются новые противовирусные препараты этой группы Валтрекс и Фамвир, в которых преодолен основной недостаток Ацикловира — низкая биодоступность при пероральном применении.
К настоящему времени более 50 млн. человек успешно прошли лечение Ацикловиром и его аналогами различными способами — местно, орально и парентерально, короткими и многолетними курсами. Следует отметить, что при длительном приеме (превентивная терапия), помимо снижения частоты рецидивов, отмечается уменьшение бессимптомного выделения вируса. Следовательно, это теоретически может снижать риск передачи вируса. Однако в ряде случаев даже на фоне длительной превентивной терапии могут возникать обострения и эпизоды бессимптомного вирусовыделения, при которых не исключена возможность неумышленного инфицирования половых партнеров. Это объясняется, прежде всего, развитием устойчивости вируса герпеса к Ацикловиру.
За последние 10 лет увеличилось число исследований, в которых показано, что изоляты вируса простого герпеса (ВПГ 2), полученные от пациенток с продолжающимися рецидивами генитального герпеса на фоне длительной супрессивной терапии (более 4 мес.), обладают резистентностью по отношению к Ацикловиру. Кроме того, ни один из существующих противовирусных препаратов не способен элиминировать вирус из организма.
Поэтому наиболее перспективным представляются методы сочетанного применения химиопрепаратов и иммунотерапии с целью стимуляции звеньев иммунной системы больных генитальным герпесом, тем самым, способствуя блокаде репродукции вируса.
Таким образом, в настоящее время являются актуальными вопросы включения в терапию рецидивирующего генитального герпеса препаратов иммуномодулирующей направленности и изучения эффективности схем комплексной терапии.
Целью данного исследования являлось изучение эффективности применения препарата Галавит (ЗАО “Центр современной медицины Медикор”, Россия) в комплексной терапии у пациентов с хронической рецидивирующей генитальной герпесвирусной инфекцией.
Материалы и методы исследования
Для исследования было отобрано 30 человек в возрасте от 16 до 65 лет с клиническими проявлениями генитальной формы герпесвирусной инфекции, резистентной к противовирусной терапии. Критериями отбора являлись: наличие анамнеза герпетического поражения половых органов; клиническая картина рекуррентного герпеса половых органов в периоде продромы или обострения, при этом не более 48 часов от момента появления высыпаний, а также полноценная контрацепция у женщин детородного возраста.
На предварительном этапе отбора методом произвольной выборки были сформированы две группы пациентов. В основную группу вошли 20 человек, которые получали базисную терапию Валтрексом по 500 мг 2 раза в день в комплексе с Галавитом — по 100 мг в/м ежедневно 5 инъекций, далее по 100 мг через день еще 15 инъекций. Контрольную группу составили 10 человек, которые получали только базисную терапию Валтрексом (табл. 1).
Таблица 1. Характеристика пациентов с ГГ, охваченных исследованием
| Группа | Общая численность | Соотношение в группе по полу, % | Средний возраст, лет | муж. | жен. | муж. | жен. |
| Основная | 20 | 35 | 65 | 38,3 | 31,5 |
| Контрольная | 10 | 40 | 60 | 40,2 | 39,6 |
Анамнестически в обеих группах средняя продолжительность заболевания (время с момента появления первого клинического эпизода) составила 3 года, частота рецидивов — не менее 6 раз в год (средняя частота по обеим группам — 8 раз в год).
До лечения всем пациентам для подтверждения наличия герпесвирусной инфекции проводилась ПЦР-диагностика (выявление ВПГ 2 в 100 % случаев).
У всех пациентов были жалобы на пузырьковые или эрозивные высыпания в области гениталий, зуд, жжение.
Все пациенты прошли комплексное клиническое и лабораторное обследование до приема препаратов, на 6-й день от начала приема и после окончания приема препаратов.
Объективное обследование включало в себя наружный осмотр места поражения. Оценивалось состояние кожных покровов и слизистых: наличие пузырьков, язвочек, корочек, гиперемии. Выяснялись жалобы пациента (зуд, жжение, общее состояние, температура, миалгия).
Для оценки степени выраженности местных симптомов больной опрашивался по следующей шкале оценок:
0. Боль и зуд отсутствуют.
1. Симптомы выражены слабо.
2. Симптомы выражены умеренно.
3. Симптомы выражены сильно.
Общая площадь поражения подсчитывалась путем суммирования размеров площадей отдельных поражений.
Лабораторное обследование включало в себя: общеклиническое исследование крови (гемоглобин, эритроциты, лейкоциты, нейтрофилы, эозинофилы, лимфоциты, моноциты, СОЭ), определение иммунного статуса (субпопуляции лимфоцитов CD3+, CD4+, CD8+, CD16+, CD25+, HLA-DR в периферической крови, содержание иммуноглобулинов А, М, G в сыворотке, ИФН-статус с определением уровня ИФН-α в сыворотке, его спонтанной и стимулированной продукции, определение спонтанной и стимулированной продукции ИФН-γ), биохимический анализ крови (общий белок, глюкоза, билирубин, АЛТ/АСТ, тимоловая проба), общий анализ мочи, идентификация возбудителя в мазках методом ПЦР.
Результаты
Оценка эффективности лечения осуществлялась по первичному и вторичным критериям. Первичным критерием служило время достижения полного выздоровления (полная реэпителизация), вторичными были время, необходимое для образования корочек, и время продолжительности местных симптомов (боль, зуд).
В основной группе больных исчезновение везикул и образование корочек на фоне лечения Галавитом отмечалось уже на третий день от начала лечения, в то время как в контрольной группе острая фаза местного воспаления купировалась лишь к пятому дню. Полная реэпителизация в основной и контрольной группах наступила к началу седьмого дня лечения. При этом возбудитель ВПГ 2 в мазках методом ПЦР не выявлялся у 97% больных основной группы и у 95% больных группы контроля. В процессе лечения препаратом свежие высыпания ни у кого не наблюдались.
Кроме того, отмечено увеличение длительности клинической ремиссии в отдаленном периоде в основной группе до 4 месяцев (в среднем до 68 дней), в контрольной группе она осталась практически без изменений — 35 дней (рис. 1).
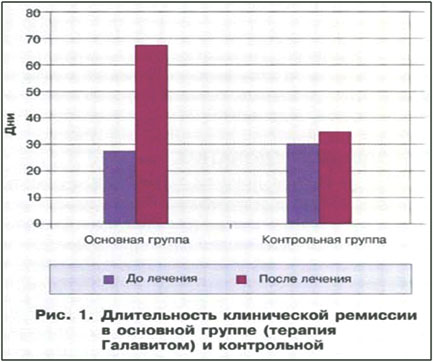
Как уже упоминалось выше, у пациентов, страдающих генитальной рецидивирующей герпесвирусной инфекцией, имеется специфический иммунодефицит, сформированный персистированием вируса герпеса в организме. Этот факт подтвердился при обследовании больных, охваченных данным исследованием, у них выявлялись лабораторные признаки вторичного иммунодефицита.
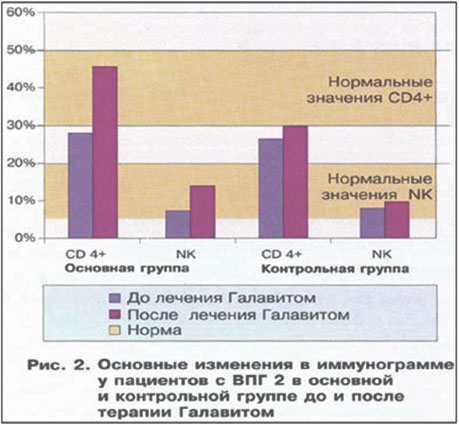
В иммунном статусе пациентов, страдающих генитальной герпесвирусной инфекцией, наиболее значимые изменения касались показателей, играющих важную роль в противовирусной защите: содержания CD4+ лимфоцитов, NK-клеток, уровня выработки ИФН-α и γ (табл. 2).
Таблица 2. Изменения в иммунограмме, наблюдаемые у пациентов с ВПГ 2 до и после лечения
| Показатели иммунограммы | Норма | До лечения | После лечения | Основная группа | Контрольная группа | Основная группа | Контрольная группа |
| CD4+,% | 31 -49 | 28,3 ± 2,6 | 27,4±2,8 | 45,4 ± 3,5* | 30,7 ± 2,6 |
| NK,% | 10- 20 | 7,2 ± 1,4 | 8,6 ± 1,3 | 14,4 ± 1,2* | 9,3 ± 1,3 |
| ИФН-γ, пкг/мл | 0-50 | 2,0 ±0,7 | 2,0 ±0,8 | 20,6 ±4,5** | 12,4 ±4,8 |
| ИФН-α, пкг/мл | 5-10 | 5,4 ± 1,2 | 4,2 ± 1,4 | 13,4 ± 2,1** | 8,2 ± 2,8 |
*Достоверно отличается от исходного значения – р<0,01.
**Достоверно отличается от исходного значения – р<0,05.
Исходно в основной и контрольной группе было снижено содержание CD4+ лимфоцитов (28% и 27% соответственно) и NK-клеток (7% и 8% соответственно). Эти изменения отражают способность вирусов герпеса угнетать ответ Т-лимфоцитов и NK-клеток, воздействуя на систему МНС (главный комплекс гистосовместимости). Кроме того, отмечалось одинаковое для обеих групп снижение уровней выработки ИФН-α и γ. Снижение продукции ИФН-α, играющего важнейшую роль в осуществлении противовирусной защиты, может способствовать развитию вирусной инфекции. Недостаточность продукции “иммуннорегуляторного” ИФН-γ отражает нарушение функциональной активности CD4+ клеток у больных с рецидивирующим генитальным герпесом, которая также вносит заметный вклад в формирование у больных иммунной дисфункции. В целом снижение реактивности клеточного звена и системы интерферона способствует хроническому часто рецедивирующему течению герпесвирусной инфекции.
При анализе влияния терапии Галавитом в основной группе отмечалось достоверное увеличение количества CD4+ лимфоцитов и NK-клеток до нормальных величин (рис. 2).

Помимо снижения количества иммунокомпетентных клеток, при герпесвирусной инфекции характерно также снижение их функциональной активности, что проявляется в снижении выработки цитокинов и, в частности, интерферонов. Так, в основной группе наблюдался подъем уровней ИФН-α и γ (рис. 3).
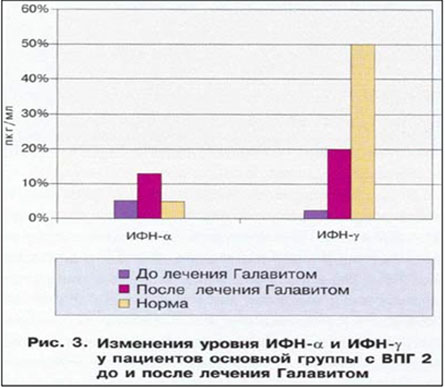
Повышение выработки ИФН-α способствует подавлению репликации вируса, увеличивая экспрессию антигенов МНС I класса, вследствие чего повышается чувствительность вирус-инфицированных клеток к цитотоксическому действию Т-лимфоцитов. Кроме того, под действием ИФН-α активируются NK-клетки, в результате чего усиливается синтез ИФН-γ являющегося важнейшим фактором в дифференцировке Т-хелперов и развитии противовирусной защиты.
В целом после приема Галавита у пациентов с хронической рецидивирующей герпесвирусной инфекцией отмечалось некоторое восстановление содержания и функциональной активности клеток (Т-хелперов, NK-клеток), участвующих в подавлении репликации вируса, что отразилось в увеличении длительности периода ремиссии.
В контрольной группе таких изменений не наблюдалось; после проведения курса базисной терапии отмечалась тенденция в сторону повышения только уровня интерферонов. По данным общеклинических и лабораторных методов исследования, побочных эффектов и осложнений при приеме препарата Галавит не выявлено.
Выводы
- Препарат Галавит оказывает иммунокорригирующее действие на систему иммунитета у больных, страдающих хронической рецидивирующей герпесвирусной инфекцией, увеличивая содержание CD4+ лимфоцитов и NK-клеток, активирующих систему интерферона.
- Применение Галавита в комплексной терапии пациентов с генитальной формой хронической рецидивирующей герпесвирусной инфекции сокращает длительность рецидивов и заметно уменьшает их частоту в отдаленном периоде.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник


