Вторичные иммунодефициты при герпесе
Комментарии
Опубликовано в журнале
Терра Медика Нова »» № 2 ’99
ИНФЕКЦИОННЫЕ БОЛЕЗНИ
В.А. Исаков, М.М. Сафронова, Ю.В. Аспель
НИИ гриппа РАМН, МАПО, Санкт-Петербург, Россия
В практической работе врачи часто встречаются с развитием у больных вторичных иммунодефицитных состояний (ИДС) различного генеза. Причиной иммуносупрессии могут быть перенесенные вирусные или бактериальные инфекции, солнечная инсоляция, переохлаждение, радиационное облучение, плохое питание, тяжелое соматическое заболевание, обширная хирургическая операция, онкологическая и гематологическая патологии и пр. ИДС характеризуется нарушениями в различных звеньях иммунитета, что способствует активации латентных вирусных и бактериальных инфекций (таких как представители семейства герпесвирусов (ГВ), аденовирусы и некоторые другие респираторные вирусы, ВИЧ, хламидии, микоплазмы). Необходимо подчеркнуть, что клинические проявления инфекции (в том числе и ГВ-инфекций), протекавшие ранее латентно, могут быть тяжелыми на фоне ИДС, с тенденцией к генерализации и возникновению осложнений, которые подчас определяют развитие и исход основного заболевания, создавая угрозу для здоровья и жизни пациента. Так, отмечено, что если у пациента с нормальной иммунной реакцией крайне редко встречаются осложнения после перенесенного простого герпеса, то после трансплантации костного мозга, которая сопровождается субтотальным облучением тела и иммуносупрессивной терапией, до 2% больных имеют поражения ЦНС, такие как вирусный асептический менингит, менингоэнцефалит, поперечный миелит или некротическая миелопатия [7].
Классификация клинических форм герпесвирусной инфекции (ГИ) у лиц с иммунодефицитными состояниями (Исаков ВА, Сафронова М.М., 1997)
I. Простой герпес
Атипичные формы
Зостериформный простой герпес (ПГ)
Герпетиформная (герпетическая) экзема Капоши
Язвенно-некротическая форма ПГ
Генерализованные формы
Висцеральная форма (менингит, энцефалит, гепатит и др.)
Диссеминированная форма (поражение многих органов и систем)
II. Ветряная оспа — опоясывающий герпес
Гангренозная форма
Геморрагическая форма (тяжелые осложнения: пневмония, энцефалит, миокардит, гепатит)
Язвенно-некротическая форма
Генерализованная форма
III. Инфекция вирусами Эпштейна-Барра
Септическая форма инфекционного мононуклеоза
Лимфома Беркитта (новообразование челюсти, поражение слюнных и щитовидной желез, других органов)
Лейкоплакии слизистых оболочек языка, полости рта, реже — половых органов
Назофарингеальная карцинома
IV. Цитомегаловирусная инфекция
Генерализованная форма инфекции
Гепатит (подострый и хронический)
Пневмония (в сочетании с бактериальными осложнениями)
Энцефалит
V. Инфекция вирусами герпеса человека 6-го и 7-го типов
Генерализованные формы инфекции
Энцефалиты
Пневмонии
Лимфаденопатии
Инфекция при острых лейкозах, развившаяся после трансплантации органов; при СПИДе, коллагенозах и др.
VI. Инфекция вирусом герпеса человека 8-го типа
Инфекция при саркоме Калоши, ассоциированной с ВИЧ-инфекцией и СПИДом
Генитальный герпес (ГГ) встречается у 6%-10% взрослых. ГВ-инфекций наблюдаются у 2% людей, среди онкологических больных — у 50%, при ВИЧ-инфекции и СПИДе — у 95% [1-3]. При этом показано, что прогностически наиболее значимо комплексное определение ДНК ВПГ-1, ЦМВ и ВГЧ-6 (метод дот-гибридизации) у больных с ВИЧ-инфекцией [2]. Доказано, что ГВ являются кофакторами активации и прогрессирования ВИЧ-инфекции и СПИДа.
Следует отметить возможную роль вируса простого герпеса-2 (ВПГ-2) (в ассоциации с паповавирусами, цитомегаловирусом, хламидиями и микоплазмами) в развитии неопластических процессов у человека, в частности рака шейки матки и рака предстательной железы. Считают, что в этом случае ВПГ-2 может выступать в качестве кофактора канцерогенеза, инициируя развитие дисплазии и поддерживая ее в состоянии стабилизации [4]. Важная роль как этиологического фактора развития дисплазии и рака шейки матки сегодня отводится вирусу папилломы человека (особенно неблагоприятно сочетание ВПГ-2 с паповавирусами), поэтому женщины с подтвержденной папилломавирусной инфекцией должны ежегодно проходить осмотр у гинеколога с выполнением цитологического исследования цервикальных мазков.
Клинические проявления основного заболевания у пациентов со злокачественными новообразованиями и с гематологическими заболеваниями сопровождаются транзиторной иммуносупрессией, которая нередко еще более усугубляется вследствие осложнений, возникающих при стандартных методах лечения данных больных (лучевая терапия, химио- и гормонотерапия, хирургическое лечение).
При ИДС меняются клинические проявления вирусных инфекций, а следовательно, и тактика врача по ведению данных больных. В частности, важны своевременная и рациональная противовирусная терапия, оптимальные схемы лечения герпеса. Если ослаблен иммунологический контроль, то не только становится невозможной полная элиминация внутриклеточно расположенного вируса, но и создаются благоприятные условия для распространения вирусов от клетки к клетке по межклеточным мостикам или экстрацеллюлярным путем, то есть для распространения и генерализации герпесвирусной инфекции (ГИ), которая протекает тяжело.
ГГ сопровождается поражением у женщин влагалища, цервикального канала, шейки и полости матки, яичников, уретры и мочевого пузыря, у мужчин — уретры, мочевого пузыря, простаты, семенников. При орогенитальных контактах инфицируются миндалины, слизистые полости рта, при аногенитальных — область ануса, прямая кишка. На фоне ИДС характерно развитие тяжелых язвенно-некротических повреждений половых органов, в том числе при СПИДе. Часто встречается регионарный лимфаденит, редко — лимфостаз и, как результат, слоновость половых органов.
Внезапное увеличение частоты рецидивов ГИ, распространение и миграция очагов поражения иногда возникают раньше, чем клинические симптомы развивающейся злокачественной опухоли любой локализации. Таких пациентов необходимо тщательно обследовать, особенно если нет других причин для развития иммунодефицита. Женщины, страдающие рецидивирующим ГГ, должны пройти осмотр у гинеколога с выполнением кольпоскопии для ранней диагностики рака шейки матки.
Клинический исход первичной ГИ в значительной мере определяется иммунным статусом организма. В то же время характер патогенетических изменений в организме больных ГГ обусловлен преимущественно возможностью интеграции генома вируса в геном клетки-хозяина, в частности в паравертебральных сенсорных ганглиях, а также тропностью ВПГ и других ГВ к форменным элементам крови и иммуноцитам. Это во многом способствует пожизненной персистенции структур ВПГ в организме больного и обусловливает изменение клеточного и гуморального иммунитета. Более того, на сегодняшний день ГИ рассматривается как инфекционная (приобретенная) болезнь иммунной системы [5], при которой длительная персистенция вируса в ряде случаев сопровождается продуктивной инфекцией ВПГ во всех видах клеток иммунной системы, что проявляется их функциональной недостаточностью и способствует формированию иммунодефицита. Нами, а также другими исследователями показано, что основная роль в формировании противогерпетического иммунитета принадлежит клеточным факторам: их состояние во многом определяет исход первичного инфицирования, частоту и напряженность рецидивов заболевания. Длительность иммунодефицита при вирусных инфекциях зависит главным образом от свойств самого вируса, а также от реактивности организма больного.
В последние годы появились сообщения, указывающие на возможность формирования резистентных штаммов ВПГ при использовании ацикловира (АЦ) [6]. Причем устойчивые к АЦ штаммы вируса герпеса чаще выделяются у больных с герпетическими пневмониями, энцефалитами, кожно-слизистой формой ГИ на фоне выраженного иммунодефицита [1-2, 7]. По нашему мнению, тестирование клинических изолятов ВПГ на чувствительность к химио-препаратам является необходимым звеном индивидуальной тактики ведения больных ГИ, особенно в тех случаях, когда имеет место тяжелое течение заболевания, а терапия неэффективна.
Противовирусная терапия герпесвирусных инфекций у лиц с иммунодефицитными состояниями [8]
I. Простой герпес
Ацикловир. Лечебные дозы: 400 мг 5 раз в 1 сут внутрь, курс 10-14 дн; 500 мг/м2 З раза в 1 сут внутривенно, курс 10 дн. Профилактическая доза: 400 мг 4 раза в 1 сут внутрь, курс несколько недель или месяцев.
Валацикловир. Лечебная доза: 500 мг 2 раза в 1 сут внуть, курс 10 дн.
Фамцикловир. Лечебные дозы: 500 мг или 750 мг 3 роза в 1 сут внутрь, курс 7-14 дн; 5 мг/кг каждые 8 ч внутривенно, курс 7-10 дн.
II. Ацикловир-резистентная герпетическая инфекция
Фоскарнет. Лечебная доза: 60 мг/кг массы тела 3 раза в 1 сут внутривенно, курс 10-14 дн.
Ганцикловир. Лечебная доза: 5 мг/кг массы тела 3 раза в 1 сут внутривенно, курс 10-14 дн.
Видарабин. Лечебная доза: 10 мг/кг массы тела 3 раза в 1 сут внутривенно, курс 10-14 дн.
III. Ветряная оспа — опоясывающий герпес
Ацикловир. Лечебные дозы: 800 мг 5 раз в 1 сут внутрь, либо 250-500 мг/м2 2-3 раза в 1 сут внутривенно, курс 7-10 дн; после трансплантации костного мозга — 500 мг/м2 3 раза в 1 сут внутривенно, курс 7-10 дн; далее 800 мг/м2 5 раз в 1 сут последующие 6 мес; при неврологических осложнениях на фоне иммунодефицита — 250-500 мг/м2 3 раза в 1 сут внутривенно, курс 7-10дн (при любых формах герпетической инфекции); при постгерпетической невралгии — 800 мг 2 раза в 1 сут внутрь, курс 3-4 мес.
Валацикловир. Лечебная доза: 1000 мг 3 раза в 1 сут внутрь, курс 7 дн.
Фамцикловир. Лечебные дозы для взрослых: 250-500 мг 3 раза в 1 сут внутрь, курс 7 дн.
IV. Цитомегаловирусная инфекция
Ганцикловир. Лечебная доза: 5 мг/кг массы тела/сут внутривенно, курс 2-3 нед. Профилактическая доза: 5 мг/кг массы тела/нед, курс 4-5 мес.
Фоскарнет. Лечебная доза: 60 мг/кг массы тела 3 раза в 1 сут внутривенно (введение в течение 2 ч), курс 10-14 дн.
Лечение герпеса у ВИЧ-инфицированных и больных СПИДом с использованием в комплексной терапии препаратов различного механизма действия имеет свои особенности. Исследование проводилось на базе городского центра по борьбе со СПИДом в С.-Петербурге.
У ВИЧ-инфицированных больных кожно-слизистая форма рецидивирующего простого герпеса отмечалась у 13 из 24 взрослых и у 16 из 47 детей. Для лечения пациентов со смешанной инфекцией (герпес в сочетании с ВИЧ-инфекцией) использовали ретровир (азидотимидин) в дозах, в 2 раза ниже рекомендуемых. Ретровир в сочетании с ацикловиром назначали постоянно или прерывистыми курсами.
Взрослые пациенты принимали ретровир в сочетании с ацикловиром (в дозе 1-2 г/сут) прерывистыми курсами в течение 2 мес. Дети в возрасте 3,5-5 лет получали ретровир в виде сиропа или в капсулах по 100 мг 3 раза в 1 сут в сочетании с ацикловиром по 200 мг 5 раз в 1 сут в течение 14 дн и далее по 200 мг 2 раза в 1 сут в течение 2 мес. На фоне лечения смешанной инфекции у взрослых и детей отмечался существенный клинический эффект, улучшались иммунологические показатели. У детей, принимавших ретровир постоянно (9-12 мес) в сочетании с ацикловиром, после лечения наблюдались более высокие показатели отношения CD4/СD8, количества CD4-лимфоцитов, иммуноглобулинов А и М, содержания гемоглобина, чем у детей, получавших противовирусные препараты прерывистыми курсами. Пo окончании приема ретровира у больных возникали рецидивы герпетической инфекции. В связи с этим мы считаем целесообразным назначение поддерживающих доз противовирусных препаратов в период клинической ремиссии герпеса у ВИЧ-инфицированных, использование противорецидивных курсов лечения, что предупреждает обострение простого герпеса и прогрессирование ВИЧ инфекции.
Таким образом, при лечении ГВ-инфекций у больных с ИДС необходимо сразу назначать более высокие дозы и более продолжительные курсы (в том числе и повторные) специфической противовирусной терапии, нередко сочетая системное и местное их применение. Наилучшие результаты дает комплексное лечение таких больных с одномоментным использованием препаратов разнонаправленного механизма действия (противогерпетические средства, антиоксиданты, препараты с антипротеазной активностью, интерфероны и их индукторы) и санацией очагов инфекции.
Литература
1. Лепков СВ. Зовиракс у онкологических больных. Алкеран, лейкеран, милеран, 6-меркаптопурин, 6-тиогуанин, веллферон, зовиракс в онкологической практике. М: ИПО «Полигран», 1994:92-6.
2. Исаков ВА, Борисова ВВ, Исаков ДВ. Герпес: патогенез и лабораторная диагностика: Руководство для врачей. СПб: Лань, 1999.192 cc.
3. Рахманова АГ, Пригожина ВК, Неверов ВА. Инфекционные болезни. Руководство для врачей общей практики. М, СПб, 1995. 302 сс.
4. Бохман ЯВ, Лютра УК. Рак шейки матки. Кишинев: Штиинца, 1991. 239 сс.
5. Баранский ИФ, Шубладзе АК, Каспаров АА, Гребенюк ВП. Герпес (этиология диагностика лечение). М: Медицина, 1986. 206 сс.
6. Брязжикова ТС, Исаков ВД, Юрлова ТИ, Голованова АК. Варьирующая чувствительность клинических изолятов вируса простого герпеса разных лет выделения к ацикловиру. Вест РАМН 1995; (9): 12-5.
7. Исаков ВА. Современные методы лечения герпетической инфекции. Terra Medica Nova 1997; (3): 2-7.
8. Исаков ВА, Ермоленко ДК, Черных МД. Терапия герпетической инфекции. СПб: Гиппократ, 1993.40 сс.
Комментарии (видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Левкова Е.А.
1
Савин С.З.
2
1 ФГБОУ ВО «Дальневосточный государственный университет путей сообщения»
2 Вычислительный Центр ДВО РАН
В статье представлены многолетние данные об особенностях течения патологии иммунной системы у детей различных возрастных групп (от 9 месяцев до 17 лет), инфицированных 4 типом герпеса – вирусом Эпштейна-Барр (ВЭБ). Убедительно продемонстрирована непосредственная связь между наличием инфекционного агента и реализацией многообразных проявлений заболеваний – от инфекционных до неопластических. Доступно разъяснены формулировки основных терминов в иммунологии и приведен диагностический алгоритм обследования детей на ВЭБ. Проведенные клинико-иммунологические исследования наглядно демонстрируют необходимость комплексного обследования детей с функциональными нарушениями в системе иммуногенеза с обязательной оценкой уровня инфекционной (вирусной) контаминации. Анализ результатов собственных клинико-иммунологических исследований позволяет предложить алгоритм комплексного обследования детей с функциональными нарушениями в системе иммуногенеза, включив в него изучение уровня вирусной нагрузки в качестве необходимого компонента.
функциональная иммунодефицитная болезнь
инфекционная индукция
герпес инфекции
вирус эпштейн-барр
1. Бархатова Т.В., Сенягина Н.Е., Краснов В.В. Распространенность маркеров герпес-вирусных инфекций при патологии почек у детей // Журнал инфектологии. – 2011. – 3 (3). — C. 46-51.
2. Дидковский Н.А., Малашенкова И.К. Синдром хронической усталости // Русский медицинский журнал. — 1997. — № 12. — С. 1.
3. Змушко Е.И., Белозеров Е.С., Митин Ю.А. Клиническая иммунология : руководство для врачей. – СПБ., 2001. – 576 с.
4. Кудин А.П. Эта «безобидная» вирус Эпштейна — Барр инфекция. Часть 3. Хроническая ВЭБ–инфекция и хронические ВЭБ–ассоциированные заболевания // Медицинские новости. — 2006. — Т. 1, № 8. — С. 25–31.
5. Лобзин Ю.В., Белозеров Е.С., Беляева Т.В., Волжанин В.М. Вирусные болезни человека. – СПб. : СпецЛит, 2015. – 400 с.
6. Малашенкова И.К., Дидковский H.A., Сарсаниа Ж.Ш. Выявление вирусоспецифических антител при хронической Эпштейна-Барр вирусной инфекции // Пятый Конгресс РААКИ. — М., 2002. — Т. 2. — С. 90.
7. Новиков Д.К. Медицинская иммунология : учеб. пособие. — Минск : Вышэйш. шк., 2005. — 301 с.
8. Новиков Д.К., Новиков П.Д. Клиническая иммунопатология. – М. : Мед. лит., 2009. – 448 с.
9. Хаитов Р.М. Вторичные иммунодефициты: клиника, диагностика, лечение // Иммунология. — 1999. — № 1. — С. 14-17.
10. Хаитов Р.М. Иммунология. – М. : ГЭОТАР-медиа, 2011. – 311 с.
11. Evans A.S., Niederman J.C. 1982. Epstein-Barr virus // Viral Infection of Humans, Epidemiology and Control. – 2-nd ed. / Ed. A.S. Evans. — New York : Plenum Medical Book Company, 1982. — P. 253-281.
12. Hiroshi K., Makoto M., Yumi Y. et al. Quantitative Analysis of Epstein-Barr Virus Load by Using a Real-Time PCR Assay // J. Clin. Microbiol. — 1999. — Vol. 37 (1). — P. 132-136.
13. Human Herpesviruses: Biology, Therapy, and Immunoprophylaxis / Eds A. Arvin, G. Campadelli-Fiume et al. – Cambridge : Cambridge University Press, 2007 : 1432. — P. 929-935.
Актуальность. До сегодняшнего времени сохраняются споры по вопросам этиопатогенеза герпетических инфекций и соотношения данного класса вирусных агентов к супрессии иммунной системы. В данном контексте необходимо дать несколько пояснений в отношении особенностей патогенеза инфекций семейства герпес. Цитируем Ю.В. Лобзина с соавторами [5]: «практически пожизненное сохранение герпесвирусов в организме человека объясняется способностью вирусной ДНК <…> изменять фенотипические свойства клеток хозяина – трансформация клеток. В результате трансформации запускаются иммунопатологические реакции, направленные против организма человека и проявляющиеся вирусиндуцированной иммуносупрессией».
Вторым понятием, требующим разъяснения, является понятие вирусиндуцированной иммуносупрессии. Представление о том, что инфекция – процесс, полностью зависимый от микроорганизма, доминирует в сознании врачей. Те же важнейшие нарушения в системе иммунитета организма, которые предшествуют ей, т.е. иммунодефициты, – игнорируются. Хотя индукция и интенсивность инфекционного процесса зависят от дозы, вирулентности, пути проникновения возбудителя, однако главным является степень недостаточности естественного или приобретенного иммунитета макроорганизма. Именно недостаточность иммунитета – относительный (к данному возбудителю) или абсолютный иммунодефицит – в каждой конкретной ситуации служит определяющим фактором развития инфекции. Инфекция, как фактор индукции, способствует реализации инфекционно-индуцированного иммунодефицита. Цитируя Д.К. Новикова [7; 8], необходимо говорить об иммунодефицитных болезнях (по МКБ-10) – болезнях иммунной системы как «врожденных (внутриутробных, антенатальных – примечание автора статьи), генетических или приобретенных структурных и/или недостаточностей какого-то звена в системе иммунитета, клинически проявляющихся рецидивами инфекции, вызванной вирусами, бактериями, грибами, паразитами». Из иммунодефицитных болезней вторичные иммунодефициты встречаются гораздо чаще первичных. Обычно вторичные иммунодефициты развиваются на фоне воздействия на организм неблагоприятных факторов окружающей среды или различных инфекций.
Продолжая цитировать «первоисточники», на которые достаточно часто опираются специалисты в области иммунологии и аллергологии, необходимо отметить, что приведенные определения касаются позднего постнатального периода. Так, в учебной литературе Р.М. Хаитова [10] под вторичным иммунодефицитом (ВИД) понимают такие нарушения иммунной системы, которые развиваются в позднем постнатальном периоде или у взрослых и, как принято считать, не являются результатом какого-то генетического дефекта. Среди ВИД условно можно выделить три формы: приобретенную, индуцированную и спонтанную.
К сожалению, именно данные определения ВИД применяются во всех возрастных группах, в том числе у детей. Достаточно своеобразно трактуются и формы ВИД, особенно спонтанная – «беспричинная». Такая трактовка уводит врача-клинициста от диагностического поиска, необходимости найти причину заболевания. Вновь обращаясь к работам Р.М. Хаитова [9; 10], необходимо отметить, что автор достаточно четко дает определение индуцированным ВИД — «это такие состояния, возникновение которых связано с какой-то конкретной причиной: рентгеновское облучение, кортикостероиды, цитостатики, травмы и хирургические операции, а также нарушения иммунитета, развивающиеся вторично по отношению к основному заболеванию (диабет, заболевания почек и печени, злокачественные процессы и т.д.). Вероятно, не полностью расшифрованный перечень причин («и т.д.») не позволяет определенной категории врачей соотнести с этим «т.д.» и инфекции! Также не рекомендуется применять неопределенные понятия, такие как «иммунодефицитное состояние», «иммунологическая недостаточность», так как их нельзя диагностировать или лечить как болезнь.

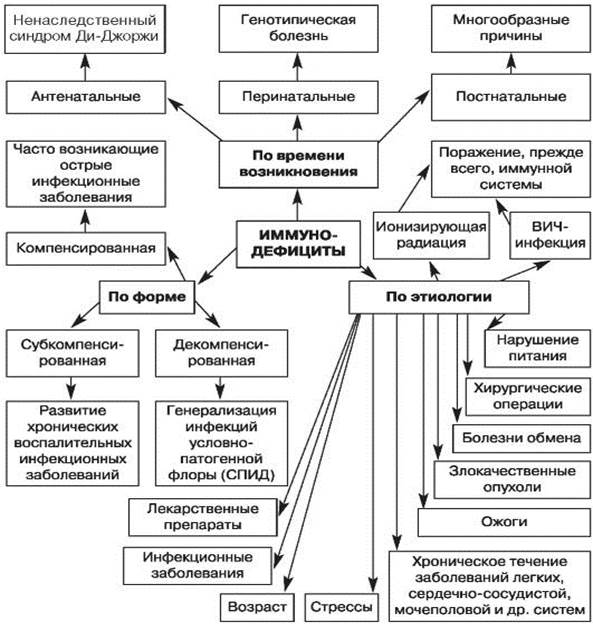
Рис. 1. Классификация вторичных иммунодефицитов по времени возникновения, этиологии, форме (по Белозерову Е.С. и др., 1992) [3]
Подводя итог в теоретической составляющей статьи – актуальности, необходимо обобщить следующее.
В педиатрии (17 лет 11 месяцев и 29 дней) в доминирующем большинстве речь идет об антенатальных и перинатальных иммунодефицитных болезнях, вторичных по отношению к анатомо-морфологическому субстрату иммунной системы – функциональных.
Таким образом, заключение врача-иммунолога должно быть сформулировано следующим образом. Антенатальная (или функциональная) иммунодефицитная болезнь, смешанного типа (или, при возможности, по отдельным звеньям, что мало вероятно), комбинированная индукция (инфекционная, гипоксическая и т.д.) с клиническими проявлениями основных синдромов – инфекционного, аллергического, аутоиммунного, неопластического и/или лимфопролиферативного.
Данные теоретические изыскания легли в основу целого цикла научно-исследовательских работ. Одно из таких исследований представлено в данной статье и посвящено исследованию иммуноиндуцирующей роли герпеса 4 типа — вируса Эпштейна-Барр у детей.
Цель: изучение особенностей клинических проявлений у детей с герпес-индуцированными формами иммунодефицитов (на примере 4 типа герпеса).
Материалы и методы. Клинико-иммунологические исследования были проведены у 320 детей в возрастном диапазоне от 9 месяцев до 17 лет. В группу исследования были также включены дети, имеющие инвалидизирующие виды патологии (детский церебральный паралич), с высоким инфекционным индексом не менее 6 раз в месяц, с неопластическими процессами, «пограничными» состояниями (лейкемоидные реакции, лимфоаденопатии). Клиническая оценка состояния здоровья детей осуществлялась в виде комплексного осмотра педиатра (номенклатура медицинских услуг). Также исследования включали в себя общелабораторные исследования — общий анализ крови, иммунологический профиль 2 уровня (реакция непрямой иммунофлюоресценции, ИФА крови), этиологические исследования (метод ИФА специфических иммуноглобулинов, ПЦР-исследования биологических субстратов – содержимое слизистых оболочек носа, зева, мочи).
Результаты собственных исследований и обсуждения. Небольшая историческая справка: двойную «фамилию» вирус получил в честь канадских ученых Мишеля Эпштейна и Эвелин Барр, так как именно им в 1964 году впервые удалось выделить его из клеток злокачественной лимфомы. Этот вирус отнесли к вирусам герпеса четвертого типа. Он имеет сложное строение и содержит ДНК. Хорошо переносит низкие температуры (до минус 70 °С) и высушивание, но быстро погибает под воздействием температуры выше 60 °С, ультрафиолетового облучения и дезинфицирующих средств. Передается вирус воздушно-капельным путем, преимущественно со слюной инфицированного человека. Возможны также гемотрансфузионный и половой пути передачи [2; 4]. Описаны случаи вертикальной передачи ВЭБ от матери плоду. Распространен вирус Эпштейна–Барр (ВЭБ) повсеместно. По статистике, в развивающихся странах и социально неблагополучных семьях большинство детей заражаются им к трем годам, а все население – к 16–18. В развитых странах такое распространение инфекции наступает чуть позже. Вирусом Эпштейна–Барр инфицировано от 80 до 100% взрослого населения любой страны. Наиболее известное и хорошо изученное заболевание, причиной которого является вирус Эпштейна–Барр – это инфекционный мононуклеоз. Ученые полагают, что этот вирус может быть причиной развития внутриутробных аномалий плода. Наряду с возбудителями токсоплазмоза, краснухи, цитомегаловирусной и герпес-инфекции первого и второго типов он входит в группу так называемых ТОRCH-инфекций. Установлено, что ВЭБ причастен к развитию аутоиммунных заболеваний, рассеянного склероза, некоторых форм гепатита, опухолей желудка, селезенки, вилочковой железы, синдрома хронической усталости и иммунной депрессии. Кроме того, он является причиной злокачественных заболеваний – лимфомы Беркитта, назофарингеальной карциномы и саркомы Капоши. Реактивация ЭБВИ (Эпштейна-Барр вирусная инфекция) и хроническое течение данной инфекции нередко развивается у пациентов со сниженной активностью иммунной системы. Наиболее характерные признаки хронической ЭБВИ – длительная субфебрильная температура тела (дольше 6 месяцев), слабость, потливость, боли в мышцах и суставах, затрудненное носовое дыхание, головокружение, нарушение сна, снижение памяти, внимания и интеллекта, эмоциональная лабильность. Как правило, эти симптомы сопровождаются увеличением лимфатических узлов, печени и селезенки. Возможно развитие пневмонии, угнетения активности костного мозга, гепатита. Исходами острой ЭБВИ, по данным И.К. Малашенкова и соавторов (2002) [6], являются выздоровление, латентная инфекция и хроническая рецидивирующая ЭБВИ. Исследованиями отечественных и зарубежных авторов установлено, что клиника хронической ЭБВИ у взрослых характеризуется наличием длительных симптомов интоксикации, лимфаденопатии, гепатоспленомегалии, тонзиллита, аденоидита, у части больных ? интерстициальной пневмонии, увеита, гепатита, патологии ЦНС и др. [2; 4; 5]. Что касается детей, то имеются лишь отдельные работы, посвященные описанию немногочисленных групп больных с хронической ЭБВИ. Кроме того, несмотря на многообразие методов лабораторной диагностики ЭБВИ (серологические методы, молекулярная гибридизация, полимеразная цепная реакция), до настоящего времени нет единства во взглядах ученых на информативность применяемых методик для определения формы и стадии инфекционного процесса.
Все дети (100%) относились к часто и длительно болеющим, при этом 72 ребенка были неорганизованными (22,5%). У 78 (24,4%) детей были зарегистрированы признаки рецидивирующей герпетической инфекции с локализацией на губах, крыльях носа, слизистой оболочке полости рта. Ежегодно 92 ребенка (28,4%) переносили бактериальные инфекции в виде тонзиллитов, пневмоний, пиелонефритов, фурункулезов, гнойных конъюнктивитов, отитов, рино-синуситов. Признаки лимфоаденопатии (микролимфоаденопатии) регистрировались у 270 детей (84,4%). У 2 детей были диагностированы неопластические процессы (один ребенок умер в 2009 году). Одна девочка с лейкемоидной реакцией наблюдается у гематоонколога в течение 2 лет. Субфебрильные реакции более 12 месяцев были зарегистрированы у 39 детей (12,2%). Грубые неврологические нарушения (преимущественно двигательные) были зафиксированы у 43 детей (13,4%) (рис. 2).
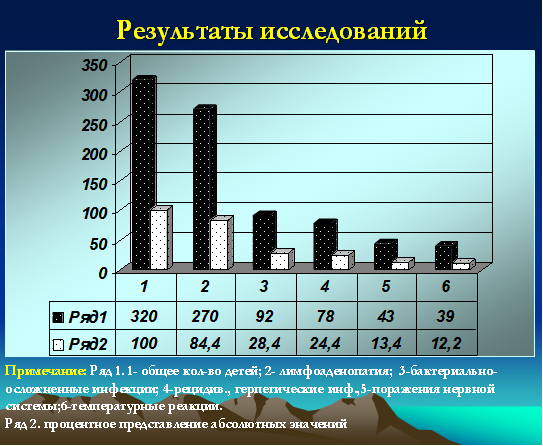
Рис. 2. Частота распределения клинических проявлений у детей с герпесиндуцированными иммунодефицитами
Иммунологические данные (в т.ч. данные лейкограммы), кроме количества лейкоцитов и лимфоцитов (абсолютное и относительное количество), носили неоднозначный характер. Классический супрессорный тип (в т.ч. и со снижением клеток цитолитической направленности) выявлялся у 108 детей (33,7%). Активация в системе клеток естественной цитотоксичности (CD16+) зафиксирована у 52 детей (16,2%). Увеличение В-клеточного пула было зарегистрировано у 38 детей (11,8%). Интересными, на наш взгляд, были полученные данные по CD95 маркеру, у 92 (28,7%) детей данный показатель был резко повышен и достигал значений 20-25%, у 30 (9,3%) детей указанный показатель не превышал 3% (рис. 3).
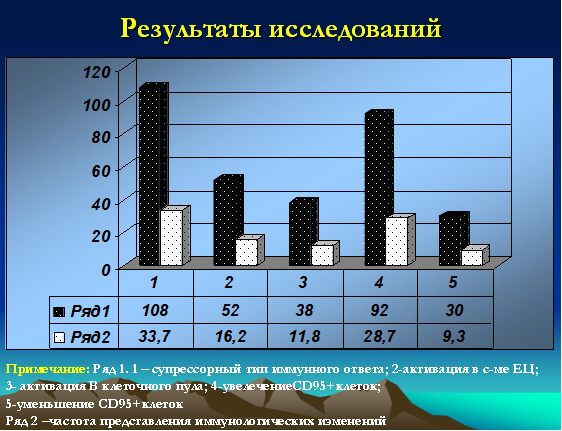
Рис. 3. Иммунологические особенности (типы распределения) у детей с герпесиндуцированными иммунодефицитами
ИФА, проведенный у детей, выявил 100% контаминацию вирусом ЭБ. Определялась следующая совокупность специфических антител:
- IgM к VCA (к капсидному антигену) – выявляются в крови в первые дни и недели болезни, максимально сохраняются до 3-4 недель;
- IgG к VCA (к капсидному антигену) – появляются в крови спустя 1-2 месяца от начала болезни, затем постепенно снижаются и сохраняются на пороговом (низком уровне) пожизненно. Повышение их титра характерно для обострения хронической ЭБВИ;
- IgM к EA (к раннему антигену) – появляются в крови в первую неделю заболевания, сохраняются в течение 2-3 месяцев и исчезают. Могут сохраняться в высоких титрах длительное время (более 3-4 месяцев), тревожно в плане формирования хронической формы ЭБВИ. Появление их при хронической инфекции служит индикатором реактивации;
- IgG к ЕA (к раннему антигену) – появляются к 3-4-й неделе заболевания, становятся максимальными на 4-6-й неделе болезни, исчезают через 3-6 месяцев. Появление высоких титров повторно указывает на активацию хронической инфекции;
- IgG к NA-1 или EBNA (к нуклеарному или ядерному антигену) – являются поздними, поскольку появляются в крови через 1-3 месяца после начала заболевания. При этом острофазные антитела выявлялись (IgM к VCA и IgM к EA) у 42 детей (13,1%), у 268 (83,7%) детей титры антител (IgG VCA + IgG к NA-1 или EBNA) значительно превышали нормативные и достигали значений более 160, у 10 (3,1%) детей диагностически значимых титров выявлено не было [9; 13] (рис. 4).
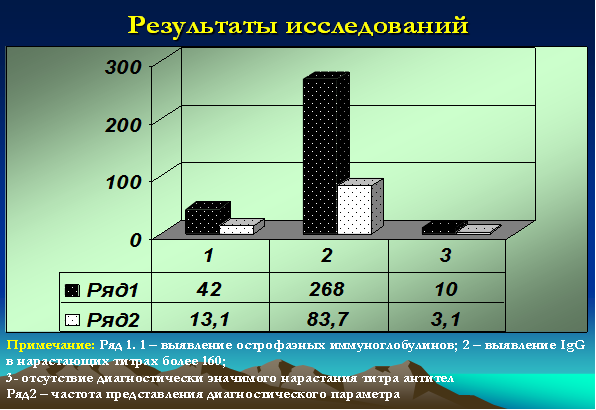
Рис. 4. Серологические исследования у детей с герпесиндуцированными иммунодефицитными болезнями
Клинические, иммунологические и этиологические сопоставления выявили следующие закономерности.
У детей с грубой неврологической симптоматикой диагностировались иммуносупрессорные изменения с резким увеличением титра антител к вирусу ЭБ. Дети, часто и длительно болеющие, имели разнонаправленные изменения: от иммуносупрессорных до активационных в системы гуморального звена, цитотоксической защиты (В-лимфоциты, иммуноглобулины класса «G», CD16+ и CD25+ клетки), уровень CD95+ клеток был преимущественно снижен.
Отдельно хочется остановиться на методах ПЦР-диагностики. В литературе активно обсуждается вопрос об использовании ПЦР для исследований на инфекции семейства герпес в различных биологических субстратах. Здесь необходимо понимать, что данный метод, особенно при использовании его для исследования плазмы, имеет свои особенности – он всегда количественный! Определение качественное не имеет смысла, так как инфекция пожизненно персистирует в организме человека. Как у больных ЭБВИ, так и у носителей может быть положительная ПЦР. Поэтому для их дифференцировки проводится ПЦР-анализ с заданной чувствительностью: для носителей до 10 копий в пробе, а для активной инфекции – 100 копий в пробе. Специфичность данного метода хоть и достигает 100%, при этом не исключает ложноположительные результаты, т.к. ПЦР-анализ информативен только при размножении (репликации) вируса, то существует и определенный процент ложноотрицательных результатов с отсутствием репликации в момент исследования [5; 9].
В результате проведенного нами исследования, ПЦР крови всегда имела отрицательный результат, даже у детей с неопластическими процессами. Распределение ПЦР-положительных результатов у детей со слизистых оболочек (ротоглотка, нос) и мочи имело следующее цифровое распределение.
Положительные реакции с 3 биологических объектов имели 36 детей (11,25%), у 62 положительные ПЦР реакции были с зева и носа – 19,38%, у 43 детей диагностировали положительный результат только с зева (13.44%), и 71 ребенок имели положительные значения ПЦР со слизистой оболочки носа (22,19%). Положительные значения только в моче имели 51 ребенок (15,94%). Остальные дети (в количестве 57) имели отрицательный результат ПЦР-исследований с биологических сред.
Дети с неопластическими процессами, длительным субфебрилитетом, лейкемоидной реакцией, лимфоаденопатией имели признаки активации хронической инфекции, резкое увеличение CD95+ клеток, положительные маркеры наличия и обострения ВЭБ в ИФА и ПЦР-исследованиях.
Таким образом, все дети имели индуцированные формы функциональной иммунодефицитной болезни, доминирующей причиной которой являлся вирус ЭБ. Проведенные предварительные клинико-иммунологические исследования наглядно демонстрируют необходимость комплексного обследования детей с функциональными нарушениями в системе иммуногенеза с обязательной оценкой уровня инфекционной (вирусной) контаминации. Выявление основных причин трактуется необходимостью применения комплексных методов лечения, в т.ч. и с применением противовирусных препаратов.
Библиографическая ссылка
Левкова Е.А., Савин С.З. ГЕРПЕС-ИНДУЦИРОВАННЫЕ ИММУНОДЕФИЦИТНЫЕ БОЛЕЗНИ У ДЕТЕЙ (НА ПРИМЕРЕ 4 ТИПА ГЕРПЕСА) // Современные проблемы науки и образования. – 2016. – № 5.;
URL: https://science-education.ru/ru/article/view?id=25135 (дата обращения: 16.10.2019).

Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник


