Что такое репликация вируса герпеса
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 19 февраля 2019;
проверки требуют 3 правки.
Герпесви́русы[3] (лат. Herpesviridae) — большое семейство ДНК-содержащих вирусов, вызывающее разнообразные болезни не только у человека и других млекопитающих, но и у птиц, рептилий, амфибий, рыб. Герпесвирусами болеют большинство населения нашей планеты[4].
Общие сведения[править | править код]
По состоянию на май 2016 года в Международном комитете по таксономии вирусов (ICTV) зарегистрированы 86 видов[2]. Отличительным признаком вирусов этого семейства является нахождение вируса в клетках латентно, персистируя, бесконечно длительное время, без клинических проявлений.
Персистенция (вирусов) (лат. persistere — оставаться, упорствовать) — термин, предложенный в 1923 году французским бактериологом, иммунологом и вирусологом Константином Левадити (Levaditi Constantin, 1874—1953) и румынским вирусологом Штефаном Николау (Nicolai Stefan, 1896—1967), обозначающий длительное сохранение вируса в организме хозяина или в клеточной культуре.
Название семейства происходит от греч. ἕρπειν (herpein) ‘ползать’ через латинское herро ‘ползаю’. Инфекционные болезни, вызванные вирусами этого семейства, протекают остро, переходят в латентную стадию, не проявляют себя до определённого времени.
При ухудшении состояния организма (простуда, стресс, утомление и т. п.) вирус даёт о себе знать болезнью. Примером может служить герпетические высыпания на губах при «простуде».
Вирусы семейства Herpesviridae имеют общие биологические свойства. Они имеют эффективные механизмы взаимодействия с иммунной системой хозяина, позволяющие им достичь максимального распространения и сохраняться в организме в течение всей жизни.
В ходе своей жизнедеятельности вирусная ДНК экспрессирует определённые группы генов и, соответственно, кодируемых ими белков, которые, собственно, и определяют жизненный цикл вируса в клетках хозяина, приводя к изменению их фенотипических свойств, то есть трансформации.
Трансформация клеток вызывает развитие определённых иммунопатологических реакций, направленных против собственного организма и приводящих к вирусиндуцированной иммуносупрессии и длительной персистенции вируса в организме человека. В клетках своего хозяина они переходят в латентное состояние. При латентном состоянии нарушается полный репродуктивный цикл вируса. Он находится в клетках хозяина в виде субвирусных структур.
Клинические формы герпесвирусных инфекций характеризуются выраженным полиморфизмом. Существуют различные формы проявления герпесвирусных инфекции.
В любом случае герпесвирусы остаются в инфицированном организме пожизненно. Вирус может периодически рецидивировать с характерными клиническими проявлениями или бессимптомно, или приобретать генерализованный характер с возможным летальным исходом.
Строение[править | править код]
Вирионы семейства вирусов герпеса имеют сферическую форму диаметром от 120 до 300 нм. Внутри зрелой вирусной частицы содержится 35—45 различных белковых молекул.
В центре вириона различают сердцевину (кор, от лат. cor) размером 75 нм, содержащую ДНК.
Эта сердцевина окружена оболочкой — капсидом. Размер капсида составляет 100—110 нм. Он построен из множества одинаковых геометрически правильных белковых структур — капсомер. Капсомеры точно подобраны и подогнаны друг к другу, образуя двадцатиугольник, по-гречески икосаэдр. Капсид содержит 162 капсомера: 150 шестиугольных (гексамеров) и 12 пятиугольных (пентамеров).
Вокруг капсида имеется аморфный белковый тегумент и всё это заключено в оболочку с гликопротеиновыми шипами.[источник не указан 2040 дней]
Геном[править | править код]
Геном герпесвирусов представляет собой линейную двухцепочечную молекулу ДНК. У герпесвируса человека 1-го типа она имеет размер 152 261 пара нуклеотидов и содержит 77 генов, все из которых кодируют белки; доля пар ГЦ составляет 68 %[5]. Геном герпесвируса человека 2-го типа состоит из 154 746 пар нуклеотидов и несёт 77 генов; доля пар ГЦ составляет 70 %[6].
Механизм инфицирования[править | править код]
Герпесвирусами заражаются человек и животные.
Образование новых вирусных частиц идёт под управлением вирусного генома. При попадании в организм носителя герпесвирусы адсорбируются клетками-мишенями на клеточной поверхности и освобождаются от капсида и дополнительной оболочки-конверта.
После эндоцитоза вирусной сердцевины происходит интегрирование вирусной ДНК с ядерным материалом клетки. Затем на ядерной мембране происходит образование и созревание новых вирионов и последующее их отпочковывание клеткой посредством экзоцитоза.
Для оболочки вируса, его капсида и ДНК, используются аминокислоты, белки, липопротеиды, нуклеозиды клетки-хозяина. По мере истощения внутриклеточных резервов, эти молекулы поступают в инфицированную клетку из межтканевых пространств.
Для культур, хронически зараженных вирусом простого герпеса, характерно[7]:
- возникновение состояния носительства после деструкции основной массы клеток и репопуляции немногих выживших;
- постоянное наличие очагов дегенерации, морфологически характерных для этого вируса;
- небольшой процент инфицированных клеток;
- низкая продукция вируса одной инфицированной клеткой;
- отсутствие интерферона в среде
- определенная резистентность клеток, освободившихся от состояния носительства, к реинфекции гомологичным вирусом.
В природе насчитывается восемь типов вирусов из семейства Herpesviridae, вызывающих болезнь у человека.
Классификация[править | править код]
Семейство герпесвирусов по классификации Международного комитета по таксономии вирусов (ICTV) делится на подсемейства. Используются критерии:
- структура генома вируса
- белковый состав
- характер репликации вируса
- среда носительства
- тропизма к тканям
- распространение вируса в культуре
- длительности репродуктивного цикла
По этим признаком различают подсемейства:
- Alphaherpesvirinae — альфагерпесвирусы, или α-герпесвирусы
- Betaherpesvirinae — бетагерпесвирусы, или β-герпесвирусы
- Gammaherpesvirinae — гаммагерпесвирусы, или γ-герпесвирусы
- 1 вид, не входящий ни в одни подсемейство и род (incertae sedis)
В 2016 году всем видам семейства изменили научное название для улучшения номенклатуры видов, при этом существенно не меняя названия герпесвирусов человека — к слову virus добавили префикс (alpha-, beta-, gamma-), указывающий подсемейство, к которому этот вид относится[8].
Герпесвирусы человека[править | править код]
Выделяют восемь типов вирусов герпеса, вызывающих разные по тяжести процесса заболевания у людей. Характерной особенностью заболеваний является нахождение вирусов в организме человека в латентном состоянии[9][10].
| Вид герпесвируса человека[3][2] | Название вируса | Подсемейство вирусов | Род вирусов | Вызываемая болезнь |
|---|---|---|---|---|
| Герпесвирус человека тип 1 (ГВЧ-1, Human alphaherpesvirus 1) | Вирус простого герпеса первого типа (ВПГ-1, Herpes simplex virus-1, HSV-1) | Альфагерпесвирусы | Simplexvirus | Оральный и генитальный герпес, но чаще оральный (герпетический стоматит, губной герпес) |
| Герпесвирус человека тип 2 (ГВЧ-2, Human alphaherpesvirus 2) | Вирус простого герпеса второго типа (ВПГ-2, Herpes simplex virus-2, HSV-2) | Альфагерпесвирусы | Simplexvirus | Оральный и генитальный герпес, но чаще генитальный и вагинальный герпес |
| Герпесвирус человека тип 3 (ГВЧ-3, Human alphaherpesvirus 3) | Вирус ветряной оспы (Varicella-zoster virus, VZV) | Альфагерпесвирусы | Varicellovirus | Ветряная оспа (варицелла, varicella), опоясывающий лишай (зостер, zoster) |
| Герпесвирус человека тип 4 (ГВЧ-4, Human gammaherpesvirus 4) | Вирус Эпштейна — Барр (ВЭБ, Epstein-Barr virus, EBV) | Гаммагерпесвирусы | Lymphocryptovirus | Инфекционный мононуклеоз, лимфома Беркитта, лимфома ЦНС у больных с иммунодефицитным синдромом, посттрансплантантный лимфопролиферативный синдром (post-transplant lymphoproliferative syndrome, PTLD), назофарингеальная карцинома |
| Герпесвирус человека тип 5 (ГВЧ-5, Human betaherpesvirus 5) | Цитомегаловирус человека (ЦМВ, Human cytomegalovirus, HCMV) | Бетагерпесвирусы | Cytomegalovirus | Инфекционный мононуклеоз, ретинит, гепатит, увеличение органов брюшной полости, воспаление слюнных желез (так называемое слюнотечение) |
Герпесвирус человека тип 6 (ВГЧ-6):
| Розеоловирусы:
| Бетагерпесвирусы | Roseolovirus | Шестая болезнь — детская розеола (розеола инфантум, roseola infantum) или экзантема (экзантема субитум, exanthem subitum) |
| Герпесвирус человека тип 7 (ВГЧ-7, Human betaherpesvirus 7) | Розеоловирус (Human herpesvirus 7, HHV-7) | Бетагерпесвирусы | Roseolovirus | Вероятная причина синдрома хронической усталости (СХУ)[3]. Часто сосуществует с вирусом герпеса 6 типа |
| Герпесвирус человека тип 8 (ВГЧ-8, Human gammaherpesvirus 8) | Герпесвирус, ассоциированный с саркомой Капоши[en] (Kaposi’s sarcoma-associated herpesvirus, KSHV) | Гаммагерпесвирусы | Rhadinovirus | Саркома Капоши, первичная лимфома серозных полостей, некоторые разновидности болезни Кастельмана |
Примечания[править | править код]
- ↑ Таксономия вирусов (англ.) на сайте Международного комитета по таксономии вирусов (ICTV).
- ↑ 1 2 3 Таксономия вирусов (англ.) на сайте Международного комитета по таксономии вирусов (ICTV). (Проверено 30 июня 2016).
- ↑ 1 2 3 Атлас по медицинской микробиологии, вирусологии и иммунологии : Учебное пособие для студентов медицинских вузов / Под ред. А. А. Воробьева, А. С. Быкова. — М. : Медицинское информационное агентство, 2003. — С. 109. — ISBN 5-89481-136-8.
- ↑ Вирусы Герпеса. Герпесвирусная инфекция
- ↑ Human herpesvirus 1, complete genome
- ↑ Human herpesvirus 2, complete genome
- ↑ Анджапаридзе О. Г., Богомолова Н. Н. Моделирование и исследование хронических форм вирусных инфекций в культурах клеток. — Москва: Медицина, 1974. — С. 161. — ISBN УДК 616.988-036.12-092.4.
- ↑ Davison A., Pellett P., Stewart J. Rename species in the family Herpesviridae to incorporate a subfamily designation : [англ.] // ICTVonline. — Code assigned: 2015.010aD. — 5 p.
- ↑ Whitley R. J. Herpesviruses. in: Baron’s Medical Microbiology (Baron S et al., eds.). — 4th. — Univ of Texas Medical Branch, 1996. — ISBN 0-9631172-1-1.
- ↑ Murray P. R.; Rosenthal K. S.; Pfaller M. A. Medical Microbiology. — 5th. — Elsevier Mosby, 2005. — ISBN 978-0-323-03303-9.
Источник
А. Кубанов, канд. мед. наук
Центральный научно-исследовательский кожно-венерологический институт МЗ РФ
В настоящее время заболевания, обусловленные вирусом простого герпеса (ВПГ), относятся к одним из наиболее распространенных: около 90% населения планеты инфицированы ВПГ. К сожалению, в России в течение многих лет проблема ВПГ оставалась вне поля зрения клиницистов и вирусологов. Во многом это объяснялось недостаточными возможностями лабораторной диагностики герпеса и отсутствием понимания патогенетических механизмов заболевания.
Заражение ВПГ может происходить воздушно-капельным или половым путем. Основными факторами, способствующими распространению заболевания, являются большое число сексуальных партнеров, пренебрежение принципами безопасного секса, низкий уровень образования, гомосексуализм. В большинстве случаев заражение половых партнеров происходит либо при их незнании о наличии инфекции, либо при аcимптомном выделении вируса у одного из партнеров. Передача ВПГ чаще осуществляется при половом контакте с больным или вирусоносителем.
Вирус может размножаться бессимптомно или продуцировать характерные для herpes labialis или генитального герпеса сгруппированные пузырьки. Состояние иммунного дефицита ведет к увеличению частоты рецидивов, более длительным периодам распространения вируса и пролонгированию симптомов.
Различают две основные антигенные группы ВПГ: 1 и 2 типа (ВПГ-1 и ВПГ-2). При этом штаммы, относящиеся к одному и тому же антигенному типу, могут отличаться по иммуногенности, вирулентности, устойчивости к воздействию различных химических и физических факторов, что в конечном итоге определяет особенности клинических проявлений болезни.
Генитальный герпес (ГГ), являясь частным случаем ВПГ-инфекции, относится к одному из наиболее распространенных заболеваний, передаваемых половым путем, и отличается от других болезней этой группы пожизненным носительством возбудителя в организме человека (латенцией), что определяет высокий процент формирования рецидивирующих форм болезни.
Герпетические высыпания на половых органах, сопровождающиеся зудом, жжением и болезненностью, повторяющиеся в течение многих лет, часто препятствуют созданию семьи, нарушают нормальную половую жизнь, могут приводить к неврастеническим и депрессивным состояниям. У женщин с тенденцией к бессимптомному течению генитального герпеса чаще наблюдаются другие осложнения — частые выкидыши и заражение плода.
Первичное инфицирование или рецидивы во время беременности могут привести к внутриутробному заражению, вызывающему повреждения, после которых дальнейшее развитие плода становится невозможным или сопровождается тяжелыми осложнениями, а инфицирование во время родов может быть причиной тяжелых неонатальных и постнатальных заболеваний новорожденных. Следствием внутриутробного инфицирования плода или интранатального инфицирования новорожденного могут быть уродства, умственное недоразвитие ребенка и даже летальный исход.
Исторически возникновение ГГ ассоциировалось с ВПГ-2, и именно по частоте выявления антител (АТ) к этому серотипу вируса при эпидемиологических исследованиях делаются выводы о распространенности инфекции. (Ранее считалось, что ВПГ-1 чаще идентифицируется при поражении кожи лица, верхних конечностей, туловища.) В настоящее время установлено, что генитальный герпес, вызываемый ВПГ-1, стал обнаруживаться гораздо чаще. Генитальная инфекция, вызванная ВПГ-1, рецидивирует сравнительно редко, более часто рецидивы возникают у больных с высоким титром антител к ВПГ-2.
Существует несколько видов клинических проявлений генитального герпеса:первичная генитальная герпетическая инфекция (в крови отсутствуют антитела к ВПГ); вторичная генитальная герпетическая инфекция (при наличии антител к ВПГ одного типа — суперинфекция ВПГ другого типа и отсутствие в анамнезе эпизодов генитального герпеса); рецидивирующая герпетическая инфекция (наличие антител к ВПГ и эпизодов генитального герпеса в анамнезе); бессимптомная герпетическая инфекция.
У большинства взрослых людей, первично инфицированных ВПГ половым путем, развивается локальная форма герпетической инфекции, ограниченная гениталиями.
Первый эпизод первичного генитального герпеса начинается без наличия циркулирующих антител к ВПГ-1 или ВПГ-2. Оба типа вирусов могут быть причиной первичного герпеса слизистых оболочек, проявляющегося гингивостоматитом, вульвовагинитом, кератитом, причем герпетическая инфекция может иметь различное течение — от легкого до тяжелого с фатальным исходом.
В начале заболевания больные могут ощущать зуд, жжение и боль в области гениталий. При типичной форме болезни пораженное место припухает, краснеет, затем на слизистых оболочках половых органов и прилежащих участках кожи появляется группа везикул размером 2-3 мм на эритематозном фоне. Пузырьки через 1-2 дня вскрываются, образуются мокнущие эрозии или язвочки, которые в дальнейшем эпителизируются под коркой или без ее образования, не оставляя рубцов.
Больных беспокоят зуд и боль в области поражения.
Длительность острого периода при первичном генитальном герпесе может достигать 3—5 недель и более. Перед появлением видимых повреждений больные могут ощущать парестезию и жжение, иногда боли, отдающие в спину и нижние конечности. Репликация ВПГ в сенсорных ганглиях может вызывать невриты, которые являются причиной сильных болей, испытываемых пациентами с генитальным герпесом. Может иметь место очень болезненное мочеиспускание, в результате инфекции уретры и слизистой оболочки мочевого пузыря часто наблюдается его задержка.
Учитывая многообразие клинических проявлений РГГ, длительное рецидивирующее течение заболевания и пожизненную персистенцию вируса в организме, его лечение остается трудным и не всегда эффективным. Следует подчеркнуть, что ни один из известных в настоящее время противовирусных препаратов не способен элиминировать вирус из организма и существенно повлиять на латентное течение заболевания.
Тактика лечения во многом определяется частотой и степенью тяжести обострений, наличием психосоциальных проблем у пациента, а также степенью риска передачи инфекции половому партнеру.
Возможность проведения противовирусной терапии должна рассматриваться во всех случаях диагностики генитального герпеса, в которой основную роль играют лабораторные методы.
Нередко при рецидивах герпеса, протекающего в атипичной форме (без выраженных клинических признаков), ошибочно диагностируется кандидоз и, наоборот, при заболеваниях, протекающих с язвенными поражениями (сифилисе, болезни Бехчета и др.), — герпес.
Целью лечения является подавление репродукции ВПГ в период обострения, формирование адекватного иммунного ответа и его длительное сохранение с целью блокирования реактивации ВПГ в очагах персистенции.
В настоящее время существуют два основных направления в лечении простого герпеса:этиопатогенетическая противовирусная терапия; комплексный метод лечения, включающий иммунотерапию (специфическую и неспецифическую) в сочетании с противовирусной терапией.
Одним из наиболее часто применяемых в противовирусной терапии препаратов является ацикловир. Доказано, что он обладает отличным профилем безопасности без значимых явлений токсичности как при кратковременном, так и при длительном использовании. Лечебная и профилактическая эффективность противовирусной терапии составляет 75—90%. При этом были установлены и многократно подтверждены совершенно уникальные для такой высокой эффективности безопасность и переносимость.
Статья опубликована в журнале «Фармацевтический вестник»
Источник
Роза Исмаиловна Ягудина, д. фарм. н., проф., зав. кафедрой организации лекарственного обеспечения и фармакоэкономики и зав. лабораторией фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Евгения Евгеньевна Аринина, к. м. н., ведущий научный сотрудник лаборатории фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Герпес (herpes simplex) — это хроническое персистирующее заболевание, характеризующееся высыпанием групп пузырьков (везикул) на коже и слизистых оболочках. Его возбудители принадлежат к семейству герпесвирусов (Herpesviridae), которое в свою очередь подразделяется на три подсемейства: α, β и γ. У человека наиболее часто встречаются нейротрофные нейроинвазивные вирусы простого герпеса (ВПГ) двух видов: ВПГ-1 и ВПГ-2, которые относятся к подсемейству α и поражают нервную систему и слизистые оболочки. Они очень эффективно обходят иммунную систему человека, чем можно объяснить длительный скрытый период болезни, позволяющий вирусу максимально распространиться в организме.
ВПГ внедряется в клетки эпителия (слизистой полости рта, глотки или половых органов), где происходит его размножение. Пораженные клетки гибнут, в очаг воспаления мигрируют лимфоциты и макрофаги, происходит выброс биологически активных веществ, повреждение капилляров и соединительной ткани. Затем вирус проникает в чувствительные нервные окончания и по центростремительным нервным волокнам — в паравертебральные ганглии. В ядрах нейронов происходит репликация вируса, цикл репродукции продолжается около 10 часов с образованием в клетке от 50 до 200 тысяч вирионов. При нормальном иммунном ответе через 2–4 недели после заражения происходит разрешение первичного заболевания и элиминация ВПГ из тканей и органов. Однако в паравертебральных ганглиях возбудитель в латентном состоянии сохраняется в течение всей жизни. В любой момент может начаться реактивация размножения ВПГ и его перемещение по нервным волокнам к месту первичного вхождения (воротам инфекции) с рецидивом специфического инфекционно-воспалительного процесса и возможной диссеминацией инфекции.
Причины возникновения и распространение вируса простого герпеса
ВПГ устойчив к действию низких температур: от –20 до –70 °С он сохраняет жизнеспособность 10 и более лет, также как и после лиофильного высушивания. Однако ВПГ не устойчив к нагреванию: при 50–52 °С инактивируется через 30 минут, а при 37 °С — в течение 10 часов. Быстрее всего вирус разрушается под действием ультрафиолетовых и рентгеновских лучей, этилового спирта, эфира и других органических растворителей, протеолитических ферментов. На поверхности кожи и на влажных предметах при комнатной температуре ВПГ сохраняет жизнеспособность в течение 1–4 часов.
Источник распространения вируса герпеса — больные и инфицированные люди. При активной (манифестной) форме он выделяется с кровью, мочой, слюной, другими биологическими жидкостями (содержимое везикул, слезы, менструальная кровь, вагинальное и цервикальное отделяемое, сперма). При латентной форме (вирусоносительстве) ВПГ выделяется таким же образом, но в меньших количествах. Носительство активного вируса чаще всего наблюдается в течение первых 12 месяцев с момента инфицирования. Но при иммунодефицитных состояниях продолжительность этого периода может увеличиваться.
От человека к человеку ВПГ передается разными путями:
- контактно-бытовым;
- половым;
- парентеральным;
- вертикальным (от матери к плоду);
- аэрозольным.
Контактно-бытовой, половой и парентеральный механизмы передачи объединяют в один, называемый «перкутанным».
Наиболее распространена передача ВПГ контактно-бытовым путем — через посуду, предметы личной гигиены, предметы быта, постельное белье, также возможно заражение при поцелуях. В зависимости от механизма передачи вируса выделяют несколько клинических форм этого заболевания. Так, к группе риска при половом и парентеральном способах передачи относятся люди, имеющие беспорядочные половые связи, употребляющие наркотические препараты.
Клиническая картина
В зависимости от участков поражения выделяют несколько клинических форм ВПГ, представленных в таблице 1.
Первичный и вторичный герпес
Заболевание может протекать в следующих формах:
- Герпес первичный
- Герпес рецидивирующий
Первичный герпес чаще всего проявляется стоматитом или фарингитом, в основном у детей и молодых людей. Его инкубационный период составляет в среднем около недели. Общие признаки для всех клинических форм ВПГ: лихорадка, озноб, увеличение регионарных лимфоузлов.
У новорожденных ВПГ протекает в виде острого гингивостоматита, сопровождающегося эрозиями, язвами, некрозом на фоне отека и гиперемии слизистых оболочек.
Факторы риска при рецидивирующей форме герпеса: повышенное физическое или эмоциональное напряжения, общее истощение организма, различные виды лихорадки, травмы, гормональные изменения, поражение кожных покровов, хронические заболевания, переохлаждение, употребление алкоголя и наркотических препаратов, беспорядочная половая жизнь. При рецидиве вирус, находящийся в латентной стадии, активируется. В результате множество вирионов продвигаются по отросткам нейрона и переходят в эпителий кожи и слизистых оболочек. Рецидивирующий герпес развивается на фоне ограниченной гиперемии, с появлением пузырьков, содержащих прозрачный экссудат. Пузырьки обычно располагаются группами, в местах первичного поражения, там же обычно возникают жжение, покалывание и болезненность. Общее состояние человека при этом обычно не изменяется, но иногда может повышаться температура. Содержимое пузырьков может ссыхаться в корку, которая затем отпадает, или пузырьки вскрываются, образуя эрозию. В среднем рецидив герпеса клинически длится около 1–1,5 недели.
После первичного заражения ВПГ навсегда встраивается в геном клетки-хозяина и никогда не элиминируется иммунной системой.
ВПГ имеет циклическую активность (в течение 2–21 дня формируются пузырьки с вирусными частицами), периоды ремиссии, во время которых язвочки пропадают. Цикл репродукции вируса составляет 10 часов. Постепенно у человека формируется противовирусный иммунитет, и частота и тяжесть рецидивов уменьшается.
Формы и симптомы вируса герпеса 1 и 2 типа

Диагностика вируса герпеса: симптомы и лабораторные исследования
Диагностика ВПГ складывается из данных клинического осмотра и результатов лабораторных исследований, особенно значимых при латентной форме.
Оральный (лабиальный) герпес легко диагностируется лишь при наличии внешних проявлений — везикул, ран или язв. На ранних стадиях, когда симптомы заболевания отсутствуют, диагностировать герпес можно только лабораторными методами, который подтверждается при выделении вируса в культуре клеток и четырехкратном повышении титра антител при активной форме заболевания.
Для подтверждения диагноза и выбора терапии используется цитологический метод (в соскобах со дна везикул, окрашенных по Райту, Романовскому — Гимзе, видны характерные для герпеса гигантские клетки с внутриядерными включениями). Однако этот метод малочувствителен и не позволяет, например, отличить ВПГ от опоясывающего лишая.
Серологический метод с IgM и иммуноточечным гликопротеином G-специфичному HSV-тесту даёт более чем 98‑процентную специфичность и позволяет, таким образом, различить HSV-1 и HSV-2 типы герпеса.
Фармакотерапия: как вылечить герпес
В настоящее время существуют два основных направления в лечении вируса простого герпеса в организме человека:
- противовирусная терапия
- комплексная — иммунотерапия (специфическая + неспецифическая) + противовирусная
Противовирусная фармакотерапия
Ацикловир — противовирусный (противогерпетический) препарат, синтетический аналог нуклеозида тимидина, обладающий высокоизбирательным действием на вирусы герпеса. Внутри инфицированных клеток под действием вирусной тимидинкиназы проходит ряд последовательных реакций трансформации ацикловира в моно-, ди- и трифосфат ацикловира. Ацикловир трифосфат встраивается в цепочку вирусной ДНК и блокирует ее синтез посредством конкурентного ингибирования вирусной ДНК-полимеразы.
Специфичность и весьма высокая селективность действия также обусловлены его преимущественным накоплением в клетках, пораженных вирусом. Эффективен для большинства видов ВПГ, но лучший эффект достигается в лечении инфекций, вызванных herpes simplex типов 1 и 2, varicella zoster, слабее влияет на вирус Эпштейна — Барр и цитомегаловирусы.
После приема внутрь биологическая доступность ацикловира составляет 15–30 %, при этом создаются дозозависимые концентрации, достаточные для эффективного лечения вирусных заболеваний. Хорошо проникает во многие органы, ткани и жидкости организма, проникает через гематоэнцефалический и плацентарный барьеры, накапливается в грудном молоке. Связывание ацикловира с белками плазмы составляет 9–33 % и не зависит от его концентрации в плазме. Пища не оказывает значительного влияния на всасывание. Побочные реакции: тошнота, рвота, диарея, преходящее незначительное повышение активности ферментов печени, небольшое повышение концентрации мочевины и креатинина, гипербилирубинемия, головная боль, головокружение, анафилактические реакции, кожная сыпь, синдром Лайелла, синдром Стивенса — Джонсона, зуд, крапивница, сыпь, в том числе сенсибилизация. Таблетки и инъекционные формы ацикловира противопоказаны детям до 3‑х лет
Валацикловир — хлористоводородная соль L-валилового эфира ацикловира. Это пролекарство в организме абсорбируется из ЖКТ и при «первом прохождении» через кишечник и/или печень вследствие ферментативного гидролиза быстро и почти полностью (99 %) превращается в L-валин и ацикловир, который после фосфорилирования приобретает специфическую активность.
Побочные реакции: тошнота, рвота, гастралгия, снижение аппетита, повышение активности ACT, головокружение, головная боль, утомляемость, почечная недостаточность, микроангиопатия, гемолитическая анемия. Не зависит от приема пищи.
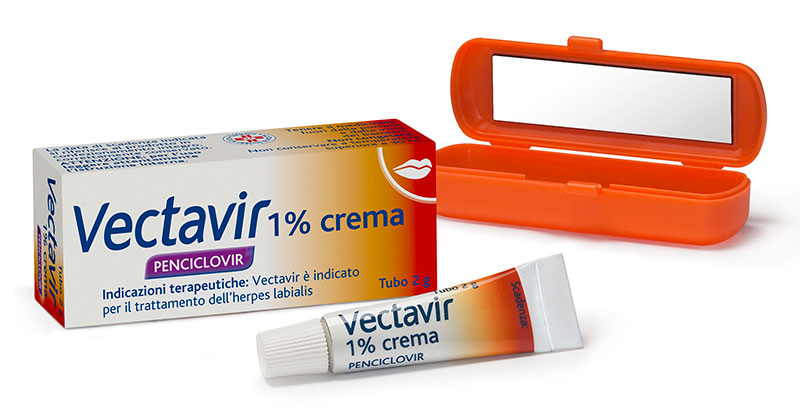
Пенцикловир — противовирусный препарат, активен в отношении вирусов herpes simplex 1 и 2 типа и varicella zoster. Пенцикловир попадает в инфицированные вирусом клетки, где под действием вирусной тимидинкиназы быстро превращается в монофосфат, который в свою очередь при участии клеточных ферментов переходит в трифосфат. Пенцикловира трифосфат находится в инфицированных вирусами клетках более 12 часов, подавляя в них синтез вирусной ДНК (дезоксирибонуклеиновой кислоты) и репликацию вирусов. Биодоступность пенцикловира — 77 %.
Побочные реакции: возможны жжение, пощипывание или онемение сразу же после нанесения препарата.
Фамцикловир — после приема внутрь фамцикловир быстро и почти полностью всасывается и превращается в активный пенцикловир.
Побочные реакции: головная боль, головокружение, повышение концентрации билирубина и активности «печеночных» трансаминаз, тошнота, рвота, диарея, боль в животе, кожная сыпь, зуд, повышенная потливость.
Ганцикловир — синтетический аналог 2′-дезоксигуанозина, который подавляет размножение вирусов герпеса. Активен в отношении цитомегаловируса человека (ЦМВ), вирусов простого герпеса 1‑го и 2‑го типа, вирусов герпеса человека 6, 7 и 8 типа, Эпштейна — Барр, ветряной оспы и гепатита В. В инфицированных клетках под действием вирусной протеинкиназы UL97 ганцикловир вначале фосфорилируется с образованием ганцикловира монофосфата, под действием клеточных киназ переходит в трифосфат, а затем подвергается медленному внутриклеточному метаболизму. Так как фосфорилирование ганцикловира в большой степени зависит от действия вирусной киназы, оно происходит преимущественно в инфицированных клетках. Рекомендуется принимать во время еды.
Валганцикловир — L-валиловый эфир (пролекарство) ганцикловира, после приема внутрь быстро превращающийся в ганцикловир под действием кишечных и печеночных эстераз. Рекомендуется принимать во время еды.
Все перечисленные выше препараты — средства «скорой помощи» при любых формах герпеса.
Иммунотерапия простого герпеса
Нарушение иммунного ответа — одно из важнейших звеньев в патогенезе простого герпеса, так как часто заболевание протекает на фоне подавления иммунных реакций. Происходит снижение общего количества Т- и В-клеток, изменение их функциональной активности, наблюдаются нарушения в макрофагальном звене иммунитета, в системе интерферона.
Неспецифическая иммунотерапия включает в себя использование:
- иммуноглобулина;
- интерферонов и индукторов интерферона;
- препаратов, стимулирующих Т- и В-звенья клеточного иммунитета и фагоцитоз.
Механизм действия иммуноглобулинов при герпесе длительное время объясняли заместительным эффектом на фоне присущей этому заболеванию несостоятельности гуморального иммунитета. В последние годы было установлено, что препараты иммуноглобулинов обладают также иммуномодулирующим и антитоксическим действием, активируют опсоно-фагоцитарные реакции.
Для лечения рецидивирующего герпеса применяют иммуноглобулин человеческий нормальный. Препарат содержит достаточное для достижения терапевтического эффекта количество специфических противогерпетических антител.
Интерферон (ИФ) — фактор естественного иммунитета, продуцируется клетками в ответ на воздействие вирусов, бактерий, чужеродных антигенов и активирует реакцию элиминации возбудителей инфекции. Помимо противовирусной активности интерферон обладает антипролиферативным и иммунорегулирующим действием. ИФ повышает неспецифическую резистентность клеток (стимулирует фагоцитоз, увеличивает активность естественных киллеров). Широкий спектр противовирусной активности, отсутствие резистентных к интерферону штаммов вирусов предопределили перспективу его использования как средства этиопатогенетической терапии простого герпеса.
Для лечения различных форм рецидивирующего герпеса используются рекомбинантный альфа-2а интерферон и созданный комбинированный препарат, который состоит из иммуноглобулинов и рекомбинантного альфа-2а интерферона в виде суппозиториев для ректального и вагинального введения.
С помощью препаратов интерферона (природных или генно-инженерных) осуществляется заместительная терапия, в результате чего может блокироваться продукция собственного эндогенного ИФ пациента. Это необходимо принимать во внимание при назначении длительных (более двух недель) курсов ИФ-терапии, особенно генно-инженерных форм. В случаях длительного назначения больным ИФ отменять их следует постепенно, снижая частоту приема до трех, далее двух раз в неделю с последующей полной отменой препарата.
Тилорон, тетрагидроксиглюкопиранозилксантен — индукторы ИФ, стимулируют выработку эндогенного ИФ в организме больного. Это объясняет терапевтический эффект перечисленных препаратов при многих вирусных заболеваниях (рецидивирующем герпесе, гриппе, аденовирусной инфекции), что позволяет рекомендовать их в комплексном лечении всех герпетических заболеваний, особенно у больных, страдающих частыми простудными заболеваниями и ОРВИ.
Специфическая иммунотерапия состоит в применении герпетической вакцины (поливалентной, тканевой, инактивированной). Лечебный эффект вакцины связан со стимуляцией специфических реакций противовирусного иммунитета, восстановлением функциональной активности иммунокомпетентных клеток и специфической десенсибилизацией организма.
Комплексное лечение вируса простого герпеса
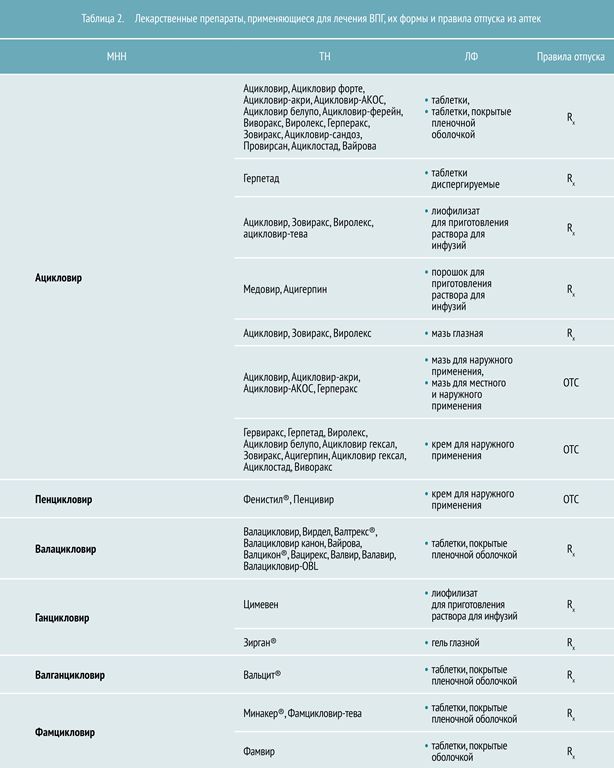
Учитывая патогенез, целесообразно использовать препараты с различным механизмом действия. Это препятствует появлению резистентных штаммов ВПГ, а применение интерферонов и их индукторов в сочетании с герпетической вакциной и иммуномодуляторами позволяет комплексно решать вопросы терапии. В таблице 2 представлены препараты, зарегистрированные на территории РФ для лечения ВПГ.Препараты при лечении вируса герпеса
Источник