Федеральные клинические рекомендации по атопическому дерматиту у детей

Год утверждения: 2016 (пересмотр каждые 3 года)
Профессиональные ассоциации:
Российская ассоциация аллергологов и клинических иммунологов (РААКИ)
1.1 Определение
Атопический дерматит (АтД) — хроническое рецидивирующее аллергическое заболевание (АЗ) кожи, возникающее, как правило, в раннем детстве и при наследственной предрасположенности.
Синонимы: атопическая экзема, синдром атопической экземы/дерматита, детская экзема, конституциональная экзема, нейродермит.
В некоторых странах Европы используют термин «атопическая экзема».
1.2 Этиология и патогенез
АтД – иммуноопосредованное заболевание со сложными механизмами развития, имеющее генетическую предрасположенность – мутация гена филаггрина нарушает барьерные функции эпидермиса.
1.3 Эпидемиология
Заболеваемость возрастает ежегодно.
Болеет 15–30 % детей и 2-10 % взрослых.
У детей АтД начинается:
- в первые полгода жизни у 45%;
- на первом году — у 60%;
- в первые 5 лет жизни – у 85%.
Риск развития респираторной аллергии при АтД — 30–80%.
Латентная склонность к развитию бронхиальной астмы (БА) у 60%, заболевают БА 30–40%
1.4 Кодирование по МКБ 10
L20.8 — Другие атопические дерматиты;
L20.9 — Атопический дерматит неуточненный;
L28.0 — Ограниченный нейродермит.
1.5 Классификация
Не существует единой общепринятой классификации АтД.
Выделяют:
- экзогенный (аллергический) АтД, ассоциированный с респираторной аллергией и сенсибилизацией к аэроаллергенам;
- эндогенный (неаллергический) АтД (5.4% — 20% больных)
Возрастные периоды болезни:
I — младенческий (до 2 лет)
II — детский (от 2 до 13 лет)
III — подростковый и взрослый (старше 13 лет)
Стадии болезни:
- Обострение: фаза выраженных/умеренных клинических проявлений
- Стадия ремиссии: неполная/полная ремиссия
- Распространенный процесс: ограниченно-локализованный; распространенный; диффузный.
Клинические формы:
- Экссудативная (I возрастной период)
- Эритемато-сквамозная (I и II периоды)
- Эритемато-сквамозная с лихенизацией (II, реже III период)
- Лихеноидная (II и III периоды)
- Пруригоподобная (II и III периоды)
Необязательно указывать в диагнозе из-за возможности сочетания нескольких форм у одного пациента.
Возрастная характеристика и локализация очагов поражения кожи
Младенческий период
Преимущественная локализация очагов:
- лицо,
- наружная поверхность голеней,
- сгибательные и разгибательные поверхности конечностей,
- к концу периода — в локтевых сгибах и подколенных ямках, на запястьях и шее.
Преобладание экссудативной формы.
Воспаление острое или подострое.
Гиперемия, отечность, мокнутие, корки.
Детский период
Преимущественная локализация очагов:
- локти,
- подколенные складки,
- задняя поверхность шеи,
- сгибы голеностопов и запястьев,
- заушные области.
Хроническое воспаление: эритема, папулы, шелушение, инфильтрация, лихенизация, расчесы, трещины.
Гипо- или гиперпигментации при угасании воспаления.
Возможно формирование дополнительной складки нижнего века — симптом Денни–Моргана.
Подростковый и взрослый период
Преимущественная локализация очагов:
- верхняя половина туловища,
- лицо,
- шея,
- верхние конечности.
Преобладают инфильтрация с лихенизацией, синюшная эритема, сплошная инфильтрация из-за сливающихся папул.
Распространенность поражения кожи:
- Ограниченно-локализованный <10% поражённой кожи: локтевые и/или подколенные складки, кожа кистей рук, кожа шеи и/или лица.
- Распространенный — 10–50%: частично кожа груди, спины, участки кожи конечностей.
- Диффузный >50%: всё тело, волосистая часть головы
Степени тяжести АтД
Учитываются следующие критерии:
- длительность и частота обострений;
- длительность ремиссий;
- распространенность процесса;
- морфологические особенности;
- интенсивность зуда;
- нарушение сна;
- эффективность терапии.
Легкая степень:
- Ограниченно локализованное поражение.
- Редкие обострения (1–2 раза в год), преимущественно в холодное время года.
- Обострение не дольше месяца.
- Продолжительность ремиссии 6–8 мес.
- Хороший эффект терапии.
Среднетяжелая степень:
- Распространенное поражение.
- Обострения 3–4 раза в год.
- Обострение по несколько месяцев.
- Продолжительность ремиссии менее 4 мес.
- Упорное течение с невыраженным эффектом терапии.
Тяжелая степень:
- Распространенное или диффузное поражение.
- Более шести обострений за год.
- Обострение по несколько месяцев или постоянное.
- Редкие ремиссии менее 2 мес.
- Лечение приносит кратковременное и незначительное улучшение
Степень тяжести оценивают также по шкалам:
- SCORAD (ScoringofAtopicDermatitis),
- EASI (ExzemaAreaandSeverityIndex),
- IGA (Investigators’ GlobalAssessment).
2. Диагностика
2.1 Жалобы и анамнез
Основные жалобы:
- интенсивный и постоянный кожный зуд,
- сухость и стянутость кожи,
- высыпания,
- покраснение, шелушение, мокнутие,
- нарушение сна и дневной активности,
- при распространенном процессе возможна общая интоксикация – повышение температуры, озноб, увеличение периферических лимфатических узлов,
- нередко присоединяется вторичная инфекция: бактериальная, грибковая или вирусная.
Анамнез
Обращается внимание на:
- начало в детстве;
- другие атопические заболевания (АР, БА);
- атопических заболеваний у родственников (больная мать – вероятность наследования 75%, больной отец – то 60%, все в семье здоровы — 15%);
- сезонность обострений;
- наличие провоцирующих факторов;
- связь обострений с воздействием аллергенов;
- сопутствующая инфекция, осложняющая течение заболевания.
2.2 Физикальное обследование
Характер и локализация высыпаний;
Расчесы (свидетельство интенсивности кожного зуда);
Признаки инфицирования кожи;
Симптомы аллергического ринита (АР), конъюнктивита и БА;
Сухость кожи;
Возрастные изменения характерных поражений кожи;
Белый дермографизм;
Склонность к кожным инфекциям;
Хейлит;
Симптом Денни–Моргана — дополнительная складка нижнего века;
Гиперпигментация периорбитальной области;
При сопутствующих заболеваниях и очагах хронической инфекции — общеклиническое обследование.
2.3 Лабораторная диагностика
Клинический анализ крови (эозинофилия).
2.4 Инструментальная диагностика
При наличии показаний: консультации гастроэнтеролога, пульмонолога, эндокринолога и др.; ЭГДС; УЗИ; рентгенологическое исследование органов грудной клетки, придаточных пазух носа; ФВД и др.
Рекомендованы консультации аллерголога, дерматолога и других.
2.4 Аллергологическое обследование
Вне обострения АтД: prick – тесты или скарификационные тесты со стандартным набором ингаляционных аллергенов.
Иммунологическое обследование (необязательно): IgА, IgМ и IgG в сыворотке для исключения селективного дефицита IgA с признаками АтД.
При диффузном процессе или других противопоказаниях к аллергологическому обследованию in vivo — лабораторная аллергодиагностика:
- уровень общего сывороточного IgE (неспецифичен);
- антител изотипа IgE к неинфекционным аллергенам или их компонентам (ИФА, РАСТ, МАСТ, ISAC).
2.5 Дифференциальная диагностика
Дерматиты: себорейный, пеленочный;
АКД;
Чесотка;
Строфулюс;
Ихтиоз обыкновенный;
Псориаз обыкновенный;
Ограниченный нейродермит (лишай Видаля);
Микробная экзема;
Розовый лишай Жибера;
Дерматофитии;
Лимфома кожи в ранней стадии;
Герпетиформный дерматит Дюринга;
Фенилкетонурия;
Синдромы гипериммуноглобулинемии E или Вискотта–Олдрича;
Десквамативная эритродермия Лейнера–Муссу.
Диагностические критерии Атопического дерматита
Обязательные признаки:
- Зуд кожи;
- Характерные морфологические особенности поражения кожи в зависимости от возраста;
- Характер воспаления (острое, подострое, хроническое);
- Хроническое, рецидивирующее течение
Важные (в большинстве случаев):
- Дебют заболевания в раннем детском возрасте;
- Атопия: сопутствующие аллергические заболевания, семейный анамнез, IgE- опосредованная сенсибилизация;
- Сухость кожи
Дополнительные:
- Атипичные сосудистые реакции (белый дермографизм, бледность лица и т.п.);
- Фолликулярный кератоз, простой белый лишай, исчерченность ладоней, сухость кожи — ксероз;
- Поражение периорбитальной области и век;
- Поражение периоральной, околоушной областей, наружных слуховых проходов, хейлит;
- Лихенизация, перифолликулярные изменения, экскориации вследствие кожного зуда
Критерии исключения:
- Чесотка;
- Себорейный дерматит;
- Пеленочный дерматит;
- Контактный дерматит;
- Ихтиоз обыкновенный;
- Т–клеточная лимфома кожи;
- Псориаз обыкновенный;
- Фоточувствительные дерматозы;
- Иммунодефицитные заболевания;
- Эритродермии другого генеза
3. Лечение
Проводится лечение вторичной бактериальной инфекции, так как АтД часто осложняется развитием пиодермий.
Преимущественная локализация поражения в воротниковой зоне, на шее, лице и волосистой части головы указывает на присоединение грибковой инфекции Malassezia spp. Назначают наружные комбинированные препараты, при их неэффективности – препараты системного действия: кетоконазол, итраконазол, тербинафин, флуконазол и др.
3.4 Физиотерапевтические методы лечения
В комплексе с наружной терапией и фармакотерапией.
Основное — ультрафиолетовое облучение при различных стадиях АтД.
Вне обострений при тяжелом хроническом течении с преобладанием зуда и лихеноидных форм применяют фототерапию:
- широкополосную UVA+UVB = 290-400 нм;
- узкополосную UVB 311-313 нм;
- UVA1 340-400 нм (можно во время обострений).
Фототерапию не назначают детям младше 12 лет.
При тяжелом и упорном течении применяют фотохимиотерапию или ПУВА-терапию — комбинация фурокумариновых фотосенсибилизаторов и длинноволнового УФО 320–400 нм.
Наиболее эффективным метод — узкополосная фототерапия.
Средние дозы UVA 1 эквивалентны узкополосной фототерапии.
Высокие дозы UVA 1 эффективны при тяжелом течении АтД.
Интерферон гамма умеренно эффективен при тяжелом АтД.
Имеется положительный опыт применения ретиноевой кислоты — алитретиноина.
Проводятся клинические исследования моноклональных антител к IgE (омализумаб), к ИЛ 4 и ИЛ 13 (дупилумаб), анти CD20 антител (ритуксимаб) и других биологических препаратов.
Клинические данные по использованию при тяжелом АтД высоких доз витамина Е и D недостаточны.
4. Реабилитация
Включает санаторно-курортное лечение в санаториях дерматологического профиля.
5. Профилактика
Профилактика направлена на сохранение ремиссии и предупреждение обострений:
- элиминационные мероприятия;
- выполнение рекомендаций по уходу за кожей даже при отсутствии признаков воспаления;
- своевременное лечение сопутствующей патологии.
Неотъемлемая часть профилактики – обучение самого больного АтД, членов его семьи, медицинских работников.
Цель обучения — сообщить пациенту с АтД и членам его семьи информацию, необходимую для максимально эффективного лечения.
Наиболее распространенная форма обучения — аллергошколы.
Занятия в аллергошколе знакомят с нормальной анатомией кожи, патогенезом заболевания, лечением и профилактикой аллергических заболеваний.
Основные положения профилактики:
- Не получено доказательств эффективности гипоаллергенных или элиминационных диет во время беременности.
- Значительно уменьшает частоту АтД у ребёнка гипоаллергенная диета во время лактации женщины из группы риска.
- Исключительно грудное вскармливание первые 4 месяца жизни ребенка из группы риска, при необходимости для докармливания разрешены гипоаллергенные смеси на основе гидролизатов молочного белка.
- Введение прикормов продуктами с низкой сенсибилизирующей активностью только после 4 месяца жизни.
- Возможна профилактика пробиотиками с лактобактериями беременных и новорожденных из групп риска.
- Обучение больных профилактическим мероприятиям и правильному уходу за кожей.
- Контроль факторов внешней среды: исключение воздействия табачного дыма; уменьшение экспозиции аллергенов в первые годы жизни; низкая влажность и адекватная вентиляция помещений; минимизация поллютантов.
Любые длительные профилактические элиминационные мероприятия ухудшают качество жизни членов семьи, поэтому включают только мероприятия с доказанной эффективностью.
Остались вопросы?
Запишитесь на консультацию к врачу, бесплатно!
Внимание! информация на сайте не является медицинским диагнозом, или руководством к действию и предназначена только для ознакомления.
Источник
В статье рассмотрены современные возможности профилактики атопического дерматита. Показано, что базисный метод профилактики и лечения обострений заболевания и увеличения продолжительности ремиссии заключается в регулярном использовании эмолентов
Введение
Влияние атопического дерматита на жизнь пациента часто недооценивается. Существует диссонанс между оценками тяжести заболевания и влияния патологии на качество жизни самим пациентом и врачом. Зуд, сухость и болезненность кожных покровов, нарушение сна — ключевые симптомы, негативно влияющие на физическое здоровье пациентов как с легким, так и с тяжелым течением заболевания. Данные факторы сказываются на таких ежедневных активностях, как работа, учеба, проведение досуга, прием ванны, надевание одежды, тем самым значительно ухудшают качество жизни пациентов с атопическим дерматитом (рис.1) [1].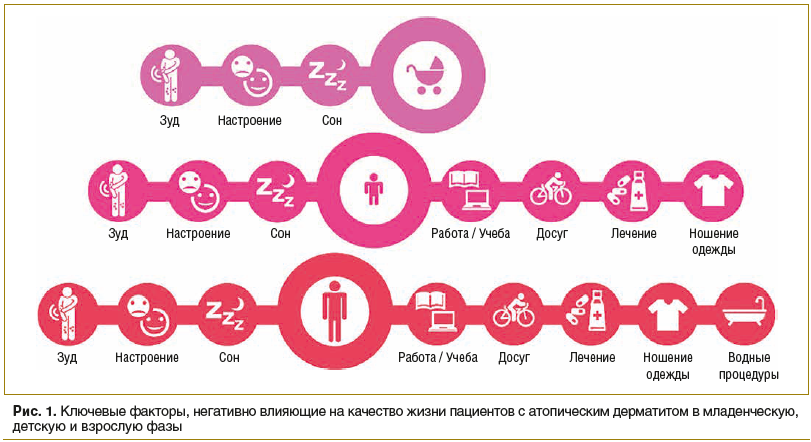
Исследования, проводимые с помощью полисомнографии, анкетирования пациентов и их родителей, актиграфии и видеомониторинга больных во время сна, показали уменьшение эффективности и продолжительности сна, а также увеличение количества ночных пробуждений. Установлено, что в среднем пациенты используют от 11 до 84 мин каждую ночь на устранение кожного зуда, а тяжесть заболевания коррелирует со степенью нарушения сна [2].
Тяжесть течения атопического дерматита ассоциирована с более высоким риском развития коморбидных заболеваний: артрита, аллергического ринита, бронхиальной астмы, аллергического дерматита [3, 4]. У пациентов с атопическим дерматитом выделяют три паттерна проявлений алиментарных аллергических реакций: неэкзематозные реакции, реакции обострения атопического дерматита и их сочетание. Неэкзематозные реакции включают крапивницу, заболевания желудочно-кишечного тракта и респираторной системы. Особенностью данных состояний, обусловленных сенсибилизацией к алиментарным факторам, является развитие клинических проявлений в течение 1–2 ч после экспозиции к аллергену. Simonsen et al. при исследовании 100 детей с атопическим дерматитом путем использования аппликационного теста установили у 47% исследуемых наличие контактной аллергии [2, 4].
Долгое время считалось, что атопический дерматит — в большей степени заболевание детского возраста. Однако исследования последних лет указывают на противоположную тенденцию. Так, Mortz et al. установили сохранение заболевания у 34,1% пациентов во взрослом периоде. Оценка дерматологического индекса качества жизни у взрослых пациентов с атопическим дерматитом во время обострений показала значительное снижение данного показателя у 66% исследуемых. Среди факторов риска перехода заболевания из детской стадии в подростковую и взрослую выделяют: ранний дебют заболевания, наличие аллергического ринита и экземы кистей [5].
Ментальное здоровье также подвергается воздействию атопического дерматита. В детском возрасте пациенты испытывают застенчивость и смущение по поводу своего заболевания. В период зрелости эти комплексы сохраняются и могут манифестировать в виде депрессии и тревожности. Коварство атопического дерматита как фактора развития заболеваний психической сферы заключается в том, что даже легкие формы данной патологии кожи могут выступать в роли триггера нарушений ментального здоровья [1].
Грамотная профилактика атопического дерматита способствует не только снижению частоты развития обострений заболевания, но и уменьшает риск формирования сопутствующих ему коморбидных заболеваний. Токсичность существующей иммуносупрессивной терапии атопического дерматита также указывает на приоритет профилактики данного заболевания [6].
Факторы, влияющие на течение атопического дерматита, его профилактика и лечение
Проактивный режим применения топических противовоспалительных препаратов как средство профилактики обострений атопического дерматита
Частое использование топических противовоспалительных средств необходимо только в случае появления новых высыпаний. Такой режим терапии атопического дерматита называется реактивным. При этом ежедневное использование эмолентов способствует значительному увеличению продолжительности ремиссии.
Другим режимом лечения заболевания является проактивный метод, когда топические глюкокортикостероиды или ингибиторы кальциневрина наносят на ранее пораженные участки кожи, а также на новые очаги продолжительное время после обострения атопического дерматита в интермиттирующем режиме (1–3 р./нед.). Эмоленты при проактивном методе лечения наносят на всю поверхность тела ежедневно [7, 8].
Образовательные программы для пациентов и их родителей
Атопический дерматит — заболевание полиэтиологической природы, лечение которого включает широкий спектр лекарственных и физиотерапевтических средств. Осведомленность пациента о патогенезе заболевания и его течении, о методах и целях лечения способствует улучшению комплаентности, нивелирует ложные предубеждения и тревожность по поводу терапии [7].
Образовательные программы могут проходить в индивидуальном или групповом формате. Самая крупная школа проводилась в Германии в 2007 г., в ней приняли участие 823 пациента. В рамках шестинедельной школы пациентам были прочитаны лекции на тему течения атопического дерматита, особенностей питания пациентов, проводились занятия с психологами, что в результате привело к снижению тяжести заболевания, оцениваемой по шкале SCORAD, по сравнению с группой контроля [9].
Ввиду высокой занятости врачей не всегда возможно проводить дни атопического дерматита в реальном времени. Поэтому другим эффективным образовательным средством для пациентов стали видеолекции врачей-дерматовенерологов, а также веб-семинары и телемедицинские конференции для пациентов, что предположительно также будет способствовать улучшению комплаентности [7].
Аллергены как фактор развития атопического дерматита
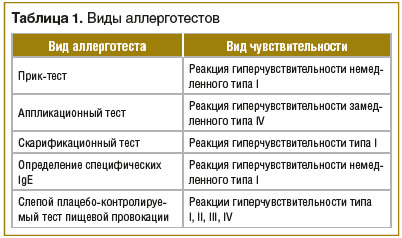
Развитие пищевой аллергии в возрасте до 2 лет является фактором риска развития тяжелого атопического дерматита. Многие авторы считают, что определение аллергенов и их устранение из окружающей среды выступает важным компонентом профилактики атопического дерматита. В пользу этого указывают данные о том, что проникновение аллергенов в кожу стимулирует выработку протеиназ эозинофилами. Это способствует формированию зуда, что может привести к развитию очередного обострения заболевания [10]. Для оценки аллергологического статуса пациента используют прик-тест, аппликационный тест, скарификационную пробу и определение уровня специфического иммуноглобулина IgE (табл. 1).
Положительный результат аппликационного теста отражает восприимчивость организма к исследуемому веществу, опосредованную через IgE-зависимую реактивность, однако это не указывает на то, что именно данный аллерген является триггером атопического дерматита. Часто экспозиция аллергена приводит к развитию немедленной реакции I типа с клинической манифестацией в виде крапивницы, зуда, нарушений работы желудочно-кишечного тракта и респираторной системы, анафилаксии, что не соотносится с проявлениями атопического дерматита. Поэтому важно установить не только наличие аллергена, но и то, что именно данный аллерген является фактором развития заболевания: прямым путем через воздействие на иммунные клетки или непрямым путем через усиление зуда [7, 9].
Реактивность к аэроаллергенам возрастает с возрастом. Наиболее часто встречающиеся аэроаллергены — продукты жизнедеятельности клещей домашней пыли, пыльца, пот домашних животных, плесневые грибы. Ингаляция аэроаллергенов приводит к секреции провоспалительных цитокинов у чувствительных пациентов, а контакт с кожей вызывает развитие экзематозной реакции у 5–45% восприимчивых больных атопическим дерматитом. Следует заподозрить наличие восприимчивости к аэроаллергенам, если высыпания у пациентов с атопическим дерматитом локализованы на открытых участках тела: на лице, шее, области декольте, верхних и нижних конечностях [2, 7, 9].
Не рекомендуется назначать всем пациентам с атопическим дерматитом гипоаллергенную диету. Установлено, что при существовании специфических IgE к белку куриного яйца исключение данного продукта из рациона пациентов с атопическим дерматитом приводит к улучшению состояния кожи. Однако другие элиминационные диеты не показали положительных результатов у больных. При подозрении на пищевую аллергию пациенту рекомендуется вести пищевой дневник. При наличии ассоциации обострений заболевания с приемом определенных продуктов рекомендуется исключение данного продукта из рациона на 4–6 нед. Если по истечении данного срока состояние пациента улучшается, необходимо провести слепой плацебо-контролируемый тест пищевой провокации, который является «золотым стандартом» диагностики пищевой аллергии (см. табл. 1).
В рамках приема практикующему врачу необходимо объяснять пациенту, что атопический дерматит — мультифакторное заболевание, в патогенезе которого аллергены играют в некоторых случаях лишь роль одного из триггеров. Поэтому профилактика должна быть комплексной, а не направленной лишь на устранение аллергенов [4, 7, 9].
Пробиотики
Доказано, что прием пробиотиков матерью во время беременности и сразу после родов снижает риск развития атопического дерматита у детей. Качественный состав пробиотиков, а именно включение одного или нескольких видов лактобактерий, не влияет на степень снижения риска развития заболевания. Исследование применения пробиотиков и пребиотиков у детей с атопическим дерматитом не показало значительного влияния на течение заболевания и риск развития обострений [10–14].
Рекомендации по модификации окружающей среды и изменению образа жизни
Важнейшие компоненты профилактики атопического дерматита — модификация окружающей среды, устранение внешних факторов, способных вызвать дебют или обострение заболевания. Окружающая среда, в которой находится беременная, также влияет на возможность развития атопического дерматита у ребенка. Установлено, что у женщин, проживающих в ремонтируемых во время беременности помещениях, риск рождения ребенка с атопическим дерматитом выше, чем в общей популяции. Летучие органические компоненты бытовых веществ способны проникать через плаценту в организм плода, вызывая активацию Th2-лимфоцитов, что лежит в основе патогенеза заболевания. Новая одежда часто содержит большое количество формальдегида, что приводит к раздражению кожи. Поэтому рекомендуется проводить тщательную обработку недавно купленных вещей. Для стирки рекомендуется использовать гелевые стиральные средства, не содержащие фосфатов. Необходимо избегать использования одежды из шерсти, шелка, фланели, т. к. данные материалы оказывают раздражающее действие на кожу. Другой важный фактор внешней среды — температура, оптимальным значением которой является диапазон между 18 и 22 °C. Резкая и частая смена температуры негативно влияет на состояние кожи детей, предрасположенных к развитию атопического дерматита. Низкий уровень влажности воздуха также может выступать в роли триггера атопического дерматита, поэтому зимой необходимо использовать увлажнитель воздуха [1, 8, 11].
Один из возможных триггеров атопического дерматита — экспозиция выделений клещей домашней пыли, чувствительность к которым среди пациентов с данным заболеванием является предметом изучения множества исследований [7, 15–19]. Bremmer et al. провели метаанализ семи рандомизированных контролируемых исследований детей, родители которых проводили специфическую санитарную обработку против клещей домашней пыли, а также использовали антиклещевые чехлы для постельных принадлежностей. Анализ показал отсутствие влияния профилактических мероприятий на вероятность развития атопического дерматита у детей. Можно предположить, что такой результат обоснован либо отсутствием участия выделений клещей домашней пыли в развитии атопического дерматита, либо недостаточностью устранения данного триггера для предотвращения заболевания [15].
Ожирение ассоциировано с более тяжелым течением атопического дерматита. Koutroulis et al. провели исследование 104 пациентов с атопическим дерматитом младше 18 лет. Было выявлено, что среди детей старше 2 лет с индексом массы тела более 24 индекс SCORAD достоверно выше, чем в других группах. Таким образом, раннее выявление и профилактика ожирения у детей предотвращают развитие атопического дерматита и способствуют снижению тяжести заболевания [12]. Оптимальный вид физических нагрузок для таких пациентов — плавание. Данный вид спорта исключает повышенную потливость и раздражение кожи одеждой. Для предупреждения раздражающего действия хлорированной воды необходимо сразу после водных процедур принять душ, а через 3–5 мин на всю поверхность тела нанести эмолент [11].
Восстановление защитных свойств кожи
Несмотря на множество теорий развития атопического дерматита, одним из ключевых факторов формирования данной патологии считается нарушение барьерной функции кожи [6, 20].
Дефекты эпидермиса являются входными воротами для потенциальных аллергенов внешней среды, что может привести к развитию реакции гиперчувствительности I типа, которая лежит в основе атопического дерматита, бронхиальной астмы, аллергического ринита и т. д. Нарушение целости эпидермиса является предрасполагающим фактором для колонизации кожи патогенными микроорганизмами, ферменты которых также повреждают эпидермис. Поэтому базисным методом профилактики, лечения обострений заболевания, а также увеличения продолжительности периода ремиссии является регулярное использование эмолентов, ежедневное нанесение которых на кожу новорожденных достоверно уменьшает риск развития атопического дерматита в будущем в 2 раза [11, 17, 19, 20].
Действующее вещество препарата Д-Пантенол (EGIS Pharmaceuticals PLC) — декспантенол — способствует восполнению субклинической дисфункции кожного барьера, а также предотвращает развитие воспалительной реакции благодаря усилению гидратации кожи и уменьшению проницаемости кожи для аллергенов (рис. 2). Ланолин и белый пчелиный воск, входящие в состав препарата, способствуют восстановлению липидного состава кожи, тем самым усиливают действие основного вещества. Препарат выпускается в двух лекарственных формах: крема и мази. Д-Пантенол является базисной ступенью терапии атопического дерматита согласно Федеральным клиническим рекомендациям по лечению данного заболевания и используется при любой степени тяжести патологии [17, 20].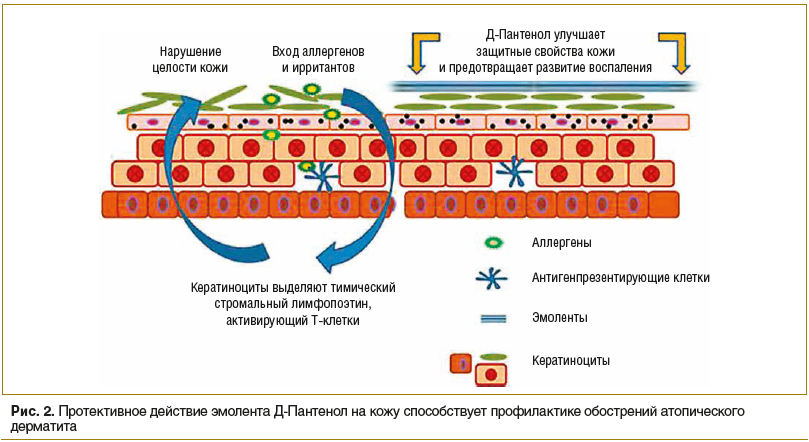
Заключение
Таким образом, профилактика атопического дерматита, ориентированная на ключевые звенья патогенеза, способствует как снижению заболеваемости самим дерматитом, так и уменьшает вероятность появления сопутствующих ему заболеваний. Так как одним из ключевых факторов развития заболевания служит нарушение барьерной функции кожи, то применение эмолентов достоверно уменьшает риск развития атопического дерматита. Современный эмолент Д-Пантенол на основе декспантенола является базисной ступенью терапии и применяется при любой степени тяжести атопического дерматита.
Источник


