Клинические рекомендации герпес у детей

Заболевание, причиной появления которого служит вирус простого герпеса (ВПГ) называется герпетическая инфекция. Оно может быть у каждого человека и даже у маленького ребенка. В этой статье мы подробно рассмотрим симптомы, клинические рекомендации и этапы лечения болезни.
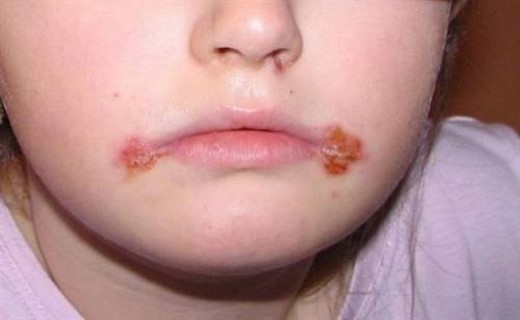
Симптомы заболевания
Приобретенная форма в 90% случаев протекает бессимптомно. При манифестном течении выделяют следующие периоды:
- инкубационный — 2 — 14 дней (в среднем 4 — 5 дней),
- начальный (продромальный),
- разгара (развития болезни),
- угасания (клинического выздоровления).
В зависимости от локализации патологического процесса различают: герпетические поражения кожи, слизистых оболочек, глаз, нервной системы, половых и внутренних органов (патологический процесс может быть изолированным и сочетанным). Наиболее часто встречаются такие симптомы герпетической инфекции, как поражения кожи и слизистых оболочек.
Клинические рекомендации о герпетической инфекции
При типичной форме кожного герпеса в начальном периоде у больного отмечаются такие симптомы: синдром интоксикации, повышается температура тела, в местах будущих высыпаний — жжение и зуд. В периоде разгара появляется характерная сыпь при герпетической инфекции: пятно, превращающееся в везикулу, наполненную серозной жидкостью. Пузырьки обычно располагаются группами на фоне гиперемии и отечности кожи, локализуясь в области каймы губ и крыльев носа, реже — на щеках, лбу, ушах, ягодицах, задней и внутренней поверхности бедер, предплечьях, кистях. Через несколько дней содержимое пузырьков мутнеет. После вскрытия везикул образуются мокнущие эрозии, которые вскоре покрываются бурыми корочками и эпителизируются. Корочки отторгаются, оставляя пигментацию. Воспалительный процесс разрешается в течение 10-14 дней.
Классификация
Типы герпетических инфекций:
А. Приобретенная герпетическая форма:
1.
Манифестная.
2.
Бессимптомная.
Б. Врожденная герпетическая форма:
1.
Манифестная.
2.
Бессимптомная.
Типы герпетических инфекций по локализации поражения:
- кожи;
- слизистых оболочек;
- глаз;
- половых органов;
- нервной системы;
- внутренних органов.
Типы инфекций по распространенности:
- локализованная;
- распространенная;
- генерализованная.
Типы герпетических инфекций:
1.
Типичная.
2.
Атипичная:
- абортивная;
- отечная;
- зостериформная;
- геморрагическая;
- язвенно-некротическая;
- герпетиформная экзема Капоши.
Типы по тяжести:
1.
Легкая форма.
2.
Среднетяжелая форма.
3.
Тяжелая форма.
Критерии тяжести:
- выраженность синдрома интоксикации;
- выраженность местных изменений.
Типы по течению:
А. По длительности:
1.
Острая (первичная)
2.
Хроническая (вторичная)
Б. По характеру:
1.
Гладкое.
2.
Негладкое:
- с осложнениями;
- с рецидивами;
- с наслоением вторичной;
- с обострением хронических заболеваний.
Лечение
Чтобы вылечить заболевание ребенку показан постельный режим, особенно при тяжелых и генерализованных формах заболевания. Диета молочно-растительная, механически щадящая при поражениях желудочно-кишечного тракта и полости рта.
В случаях локализованных кожных форм, протекающих легко, с необширными поражениями и редкими рецидивами (1 раз в 6 мес. и реже), можно ограничиться симптоматическими препаратами, которые обладают дезинфицирующим, подсушивающим, эпителизирующим действием (1 — 2% спиртовые растворы бриллиантового зеленого, метиленового синего, 3% перекиси водорода). У больных с частыми рецидивами (1 раз в 3 мес. и более) проводят этапное лечение: купирование острого процесса в период рецидива и проведение противорецидивной терапии в период ремиссии.
Этиотропная терапия
Чтобы провести лечение, в качестве этиотропной терапии используют препараты, блокирующие репликацию вирусов за счет нарушения синтеза их нуклеиновых кислот (ацикловир, теброфен, бонафтон, рио-доксол, идоксуридин, видарабин). При локализованных формах с редкими рецидивами назначают противогерпетические лекарства местно в виде капель, кремов, мазей. При частых рецидивах их применяют внутрь и парентерально. Лечение герпетической инфекции у детей необходимо назначать как можно раньше, до появления пузырьков, и продолжать до эпителизации эрозий. Доза и курс лечения зависят от длительности болезни, локализации и распространенности поражения, частоты рецидивов.
Патогенетическая терапия
Направлена на нормализацию функций иммунной системы, в том числе интерфероновой защиты. Чтобы провести лечение назначают интерфероны: человеческий лейкоцитарный (в виде аппликаций), при тяжелых генерализованных формах с поражением ЦНС — рекомбинантные (реаферон, берофор, роферон, виферон, велферон).
Используют индукторы интерферона (интерфероногены): циклоферон, полудан, неовир.
В схеме лечения применяют иммуномодуляторы: тимоген, тактивин, тималин, дибазол, метилурацил, нуклеинат Na, витамины С, А, Е; растительные адаптогены — элеутерококк, женьшень, китайский лимонник.
При лечении офтальмогерпеса, герпетического энцефалита и герпетического стоматита (у детей с первичной формой заболевания) особенно эффективен специфический иммуноглобулин.
Нестероидные противовоспалительные средства (индометацин, вольтарен, мефенаминовая кислота), которыми проводят лечение герпетической инфекции у детей, применяют при выраженном отеке, чувстве жжения, зуде.
Симптоматическая терапия
Всем больным проводят симптоматическую терапию. Антибиотики назначают при генерализованных формах и наслоении бактериальной флоры.
Противорецидивная терапия
В период ремиссии проводят противорецидивную терапию: обработку противовирусными мазями (кремами) ранее пораженных участков, назначение противовирусных препаратов или индукторов интерферона, неспецифических иммуномодуляторов, растительных адаптогенов, витаминов А, С, Е. Взрослым больным в период стойкой ремиссии возможно проведение вакцинотерапии герпетической поливакциной.
Диспансерное наблюдение рекомендуется только для детей с иммунодефицитными состояниями. Осмотр осуществляет врач поликлиники 1 раз в 3 — 6 мес. в зависимости от степени выраженности иммуносупрессии.
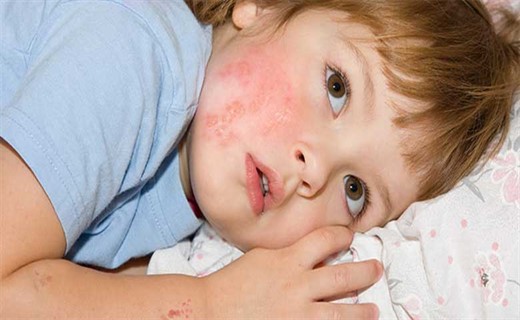
Лекарственные препараты
Противогерпетические (теброфен, риодоксол, идоксуридин, видарабин, ацикловир, валацикловир, фамацикловир) и противоцитомегаловирусные (ганцикловир, фосфоноформат) препараты блокируют репликацию, то есть нарушают синтез нуклеиновых кислот вируса.
Противогерпетические лекарства имеют следующий спектр действия:
- Herpes simplex (типа 1 и 2), Varicella zoster, аденовирусы.
- Риодоксол – оказывает дополнительно противогрибковое действие (микроспория, трихофития, кандидоз).
- Ацикловир, фамацикловир и валацикловир – дополнительно влияют на вирус Эпштейн-Барра, человеческий вирус герпеса 6-го типа, и слабо – на цитомегаловирус.
- Ганцикловир и фосфоноформат влияют – на цитомегаловирус.
- Фосфоноформат – на вирус иммунодефицита человека.
Фармакокинетика противогерпетических препаратов
Противогерпетические препараты теброфен и риодоксол – применяют местно, в виде мази. Идоксуридин – практически используют только местно:
- при заболевании глаз – раствор препарата капают в конъюнктивальный мешок через 1 ч днем и через 2 ч ночью;
- при постгерпетической невралгии. От внутривенного введения идоксуридина сейчас отказались из-за очень высокой токсичности.
Видарабин применяют местно, а при диссеминированной герпетической инфекции (энцефалит) вводят внутривенно капельно. Но препарат плохо растворяется, поэтому его инфузия в большом количестве жидкости длится около 12 ч, что нежелательно для больного с энцефалитом, отеком мозга.
Проникновение видарабина через гематоэнцефалический барьер составляет примерно 30% от концентрации препарата в плазме крови. В печени происходит превращение препарата в арабинозин гипоксантин, этот метаболит сохраняет активность и быстр0 распределяется в тканях. Элиминация происходит с мочой (50%) и калом (50%).

Ацикловир, валацикловир, фамацикловир и ганцикловир – внутрь во время еды, а также вводят внутримышечно (только ацикловир) и внутривенно (только ацикловир, ганацикловир и фамацикловир).
Биоусвоение из желудочно-кишечного тракта равно 15 — 20% (для валацикловира – 54 %), тем не менее этого достаточно для оказания эффекта. У препаратов лечения высокая активность, и они обладают способностью избирательно накапливаться в клетках, инфицированных вирусом, но не в тканях. Их концентрация в инфицированных клетках может быть в 30 — 120 раз больше, чем в плазме крови. Это важное обстоятельство объясняет значительно большую широту терапевтического действия данных препаратов по сравнению с другими и меньшую опасность возникновения осложнений.
Связывание с белками плазмы крови всего 9-30%, поэтому препараты хорошо проникают в различные ткани и жидкости (включая и ликвор). В организме человека валацикловир (1-валиновый эфир ацикловира) быстро и почти полностью превращается в ацикловир и валин под действием фермента валацикловиргидролазы. 10-15% ацикловира и ганцикловира подвергается биотрансформации в печени.
Большая часть препаратов (80 – 90 %) в неизмененном виде и в виде метаболита 9-карбоксиметоксиметилгуанина выводится почками. Период полуэлиминации примерно 3,3 ч, однако при почечной недостаточности он может увеличиваться до 20 ч, поэтому необходимо корректировать их дозированияе. Так, при Cl кр < 70 мл/ мин – дозу препаратов лечения снижают в 2 раза; при Cl кр < 50 мл/мин – дозу уменьшают еще на 1/3; при Cl кр < 25 мл/мин – еще на 1/2; и при Cl кр < 10 мл/мин – в 3 раза. Фосфоноформат (фоскарнет) – вводят внутривенно. Период его полуэлиминации от 2 до 4 ч. Экскреция осуществляется в неизмененном виде почками.
Побочные эффекты противогерпетических препаратов
Противогерпетические и противоцитомегаловирусные препараты имеют побочные эффекты:
1.
Видарабин:
- диспепсические расстройства;
- атаксия, тремор, миоклонус, галлюцинации;
- панцитопения, мегалобластоз;
- отек мозга.
2.
Ацикловира, фамацикловира и валацикловира:
- энцефалопатические реакции (тремор, летаргия, головная боль, галлюцинации, судороги);
- артериальная гипотензия;
- диспепсические явления (при назначении внутрь);
- нарушения функции печени иммунитета, кроветворения;
- при внутривенном введении – флебит, образование кристаллов в почечных канальцах.
3.
Ганцикловира:
- гематотоксичность (нейтропения, лейкопения, тромбоцитопения);
- энцефалопатические реакции;
- иммунодепрессия;
- повреждение репродуктивной функции у мужчин и женщин;
- мутагенный, тератогенный и канцерогенный эффекты.
4.
Фосфоноформата:
- костно-мозговые депрессии;
- иммунодепрессия;
- нарушения функции печени и почек;
- тератогенный, мутагенный и канцерогенный эффекты.
Взаимодействие потивогерпетических препаратов с другими препаратами
Все названные препараты, которые назначают, чтобы провести лечение герпетической инфекции у детей, являются цитостатическими, поэтому при лечении вирусных заболеваний в некоторых случаях их следует сочетать с иммуностимуляторами и с интерфероногенами (например, с циклофероном и др.), а также с иммуноглобулинами (например, с цитотектом и др.) и с препаратами, стимулирующими кроветворение (например, с филграстином и др.)
При использовании противогерпетических и противоцитомегаловирусных средств каждые 2 дня необходимо делать анализ крови. Выраженная нейротропения (меньше 500/мкл) и тромбоцитопения (меньше 25000/мкл) являются показанием для срочной отмены этих препаратов.

Осложнения
В остром периоде осложнения имеют в основном, неспецифический характер и обусловлены наслоением вторичной бактериальной флоры. При тяжелых поражениях герпетической этиологии возможно развитие специфических осложнений и формирование резидуальных явлений (очаговая неврологическая симптоматика, минимальная мозговая дисфункция церебро-астенический синдром, слепоте рубцовое сужение пищевода, слоновость половых органов, карцинома шейки матки, привычное невынашивание беременности).
Врожденная герпетическая инфекция
Внутриутробное инфицирование плода может происходить в том случае, если у матери во время беременности наблюдается первичное инфицирование или рецидив, сопровождающийся вирусемией. Возможно заражение восходящим путем при генитальном герпесе. Герпетическая инфекция у матери является фактором риска невынышиваемости беременности и перинатальной патологии ребенка. При заболеваний матери в:
- I триместре беременности возможны выкидыши,
- во II триместре — мертворождение и пороки развития (микроцефалия, слепота, атрезии различных отделов желудочно-кишечного тракта и др.),
- в III триместре — врожденная инфекция новорожденного.
Симптомы герпетической инфекции у детей не всегда проявляются поражением кожи и слизистых оболочек. Часто заболевание протекает как манифестное заражение; преобладают генерализованные формы с признаками менингоэнцефалита, гепатита, пневмонии, поражения желудочно-кишечного тракта. У детей, не получавших этиотропной терапии, летальность составляет 65%.
Особенности герпетической инфекции у детей раннего возраста
Заражение новорожденных происходит от больной матери интранатально или непосредственно после рождения, а также от персонала родильного дома. Заболевание чаще развивается на 5 — 10-й дни жизни, протекает с высокой лихорадкой (до 39 — 40° С), резко выраженной интоксикацией (рвотой, бледностью кожи, акроцианозом, одышкой, беспокойством или заторможенностью). Первично поражается слизистая оболочка полости рта, в горле, затем появляются герпетические высыпания на коже. У детей с предшествующим поражением кожи (экзема, нейродермит) возможно развитие герпетиформной экземы Капоши. Иногда наблюдаются такие симптомы: судороги, редко — потеря сознания, геморрагические высыпания, диарейный синдром. Течение болезни имеет генерализованный характер с вовлечением в патологический процесс ЦНС и внутренних органов. Летальность высокая, смерть часто наступает при явлениях инфекционно-токсического шока.
Профилактика
Большое значение в профилактике герпетической инфекции имеет санитарно-просветительная работа по формированию гигиенических навыков, закаливание, а также устранение факторов, способствующих активации герпетической инфекции (стрессовые ситуации, избыточная инсоляция, физические перегрузки, очаги хронического заражения). Особое внимание необходимо уделять детям, страдающим экземой и мокнущими формами атопического дерматита. Роженицам, имеющим герпетические высыпания на гениталиях, рекомендуют проведение кесарева сечения. Новорожденным в случае контакта с больными герпетической инфекцией следует назначать специфический противогерпетический иммуноглобулин.
Доктор Комаровский о герпетической инфекции
Источник
В последние годы среди основных возбудителей вирусных инфекций у детей особое место занимают герпес-вирусы, что связано с их повсеместным распространением, широким разнообразием, полиорганностью поражения, многообразием клинических проявлений, а также высокой частотой хронического течения. Герпес-ассоциированные заболевания входят в число наиболее распространенных и плохо контролируемых инфекций человека. Это связано с тем, что герпес-вирусы могут длительно бессимптомно циркулировать в организме человека с нормальной иммунной системой, а при иммуносупрессии способствовать развитию тяжелых заболеваний, вплоть до угрожающих жизни генерализованных инфекций. Так, по данным Всемирной организации здравоохранения (World Health Organization, WHO), смертность от герпетической инфекции составляет около 16% и находится на втором месте после гепатита среди вирусных заболеваний [1].
.jpg)
Герпес-вирусы (от греч. ?ρπειν (herpein) — ползать) — семейство ДНК-вирусов, объединены в семейство Herpesviridae, которое включает в себя 8 классифицируемых видов вирусов человека: вирусы простого герпеса — вирус простого герпеса (ВПГ-1) и вирус генитального герпеса (ВПГ-2), вирус варицелла зостер, вирус Эпштейна–Барр, цитомегаловирус, вирус герпеса человека 6-го, 7-го, 8-го типов, а также около 80 неклассифицируемых вирусов герпеса человека и животных. К подсемейству α-герпес-вирусов относятся ВПГ-1, ВПГ-2 и вирус варицелла зостер, которые характеризуются быстрой репликацией в различных типах клеток и обладают цитопатическим действием на культуры инфицированных клеток. Бета-герпес-вирусы (цитомегаловирус, вирусы герпеса 6-го и 7-го типов) также поражают различные виды клеток, приводят к увеличению их размеров (цитомегалия), могут способствовать развитию иммуносупрессивных состояний. К подсемейству γ-герпес-вирусов относятся вирус Эпштейна–Барр и вирус герпеса 8-го типа — вирус, ассоциированный с саркомой Капоши (KSHV). Их характеризует тропность к лимфоидным клеткам (Т- и В-лимфоцитам), в которых они могут длительно персистировать. В некоторых случаях способны вызывать развитие лимфомы, саркомы [2].
Для синтеза вирусных белков и образования оболочки вируса, его капсида и ДНК «дочерних» вирионов необходимы аминокислоты, липопротеиды и нуклеозиды клетки-хозяина. По мере истощения внутриклеточных резервов эти молекулы поступают в инфицированную клетку из межтканевых пространств. В связи с тем, что герпес-вирусы напрямую зависят от интенсивности внутриклеточного обмена организма человека, они колонизируют преимущественно клетки эпителия, слизистых оболочек, крови и лимфоидной ткани, которые обладают наиболее высоким темпом обмена веществ.
Вирионы герпес-вирусов термолабильны — они инактивируются в течение 30 мин при температуре 50–52 °C, в течение 20 ч — при температуре 37,5 °C, но хорошо переносят лиофилизацию. На металлических поверхностях (монеты, дверные ручки, водопроводные краны) герпес-вирусы выживают в течение 2 ч, на пластике и дереве — до 3 ч, на влажных медицинских материалах (вата и марля) — до их высыхания при комнатной температуре (до 6 ч). Уникальность герпес-вирусов заключается в том, что они способны непрерывно или циклично размножаться в инфицированных клетках тропных тканей (персистенция), а также пожизненно сохраняться в морфологически и иммунохимически видоизмененной форме в нервных клетках регионарных нервных ганглиев (латенция) и реактивироваться под влиянием различных экзо- и эндогенных провоцирующих факторов. Однако способность к персистенции и латенции у различных штаммов неодинаковая: наиболее активны в этом отношении вирусы простого герпеса, наименее — вирус Эпштейна–Барр.
По данным многочисленных исследований, к 18 годам более 90% жителей городов инфицируются одним или несколькими штаммами вирусов. Основной путь инфицирования — воздушно-капельный, при прямом контакте или через предметы обихода (общие посуда, полотенца, носовые платки и пр.). Отмечается также оральный, генитальный, трансфузионный, трансплантационный и трансплацентарный пути передачи инфекции. ВПГ 1-го и 2-го типов, цитомегаловирус входят в число возбудителей TORCH-инфекций, способствуют развитию серьезных заболеваний новорожденных и детей младшего возраста. Вирусы простого герпеса, цитомегаловирус, вирус Эпштейна–Барр рассматриваются как индикаторы СПИДа в связи с их частым обнаружением при данном заболевании [3, 4]. С герпес-вирусами связывают развитие синдрома хронической усталости (Chronic fatigue syndrome — CFS) [5].
Клинически герпес-инфекция у детей может протекать в виде ветряной оспы (вирус варицелла зостер), инфекционного мононуклеоза (вирус Эпштейна–Барр), внезапной экзантемы (вирус герпеса человека 6-го и 7-го типов), афтозного стоматита (ВПГ 1-го или 2-го типа), мононуклеозоподобного синдрома (цитомегаловирус). У подростков и взрослых людей часто инфекция протекает бессимптомно, что объясняется как биологическими свойствами штаммов, так и индивидуальными особенностями иммунного ответа. Часто при снижении иммунореактивности организма герпес-вирусы выступают в качестве вирусов-оппортунистов, приводя к более тяжелому течению основного заболевания, развитию осложнений. Велика роль герпесвирусных инфекций, особенно цитомегаловирусной, в формировании младенческой смертности. Наибольшую угрозу для жизни и здоровья детей представляют герпетические нейроинфекции — летальность при них достигает 20%, а инвалидизация — 50%. Тяжело протекают офтальмогерпес (развитие катаракты или глаукомы — до 50%), генитальный герпес, генерализованная форма Эпштейна–Барр-вирусной инфекции (инфекционного мононуклеоза) [1, 6].
Герпесвирусная инфекция относится к трудноконтролируемым заболеваниям. Несмотря на разнообразие лекарственных препаратов, использующихся для лечения данной патологии, средств, обеспечивающих полное излечение, не существует. Это обусловлено генотипическими особенностями возбудителя, формированием резистентности герпес-вирусов и молекулярной мимикрией.
Открытые с помощью методов молекулярной биологии механизмов репликации герпес-вирусов, а также изучение взаимодействия вируса с клеткой позволили создать целый ряд эффективных химиотерапевтических средств, обладающих противогерпетической активностью. Однако, эффективно купируя острые проявления инфекции, они не предотвращают рецидивирования, не всегда снижают частоту рецидивов.
Учитывая, что при герпес-ассоциированных инфекциях, как и при других хронических заболеваниях с длительной персистенцией вируса, развиваются иммунодефицитные состояния, для повышения эффективности лечения в схемы терапии наряду с противовирусными препаратами приходится включать препараты, способствующие коррекции иммунного статуса больного. Все это диктует необходимость правильно подбирать лекарственное средство, его дозу и длительность приема, при необходимости использовать комбинацию различных препаратов, избегая при этом полипрагмазии. Определенную сложность терапии в детском возрасте вызывают возрастные ограничения для ряда лекарственных средств, наличие нежелательных лекарстввенных реакций (НЛР) и противопоказаний.
В настоящее время для лечения герпесвирусных заболеваний и профилактики рецидивов используют следующие группы препаратов (табл.).
При лечении герпес-инфекций следует придерживаться комплексного подхода. Длительность и интенсивность терапии определяются возрастом больного, клинической формой заболевания, тяжестью его течения, а также наличием осложнений и сопутствующей патологии. Лечебно-профилактические мероприятия следует разделять на несколько этапов.
- Острый период болезни (рецидив) — охранительный режим, лечебное питание, противовирусные препараты, интерфероны и их индукторы. По показаниям назначаются иммуноглобулины, антибактериальные препараты местного и системного действия, глюкокортикоиды, нейро- и ангиопротекторы, гепатопротекторы, кардиотропные препараты, ингибиторы протеаз. Симптоматическая терапия может включать жаропонижающие, отхаркивающие и муколитические препараты.
- Ремиссия, стихание основных клинических проявлений (иммуномодуляторы, адаптогены растительного происхождения, пре- и пробиотики, витамино-минеральные комплексы).
- Профилактика рецидивов (специфическая профилактика — вакцинация, санация хронических очагов инфекции, восстановление иммунного статуса и пр.).
Следует отметить, что сочетанное применение противовирусных препаратов и иммунобиологических средств имеет ряд преимуществ. Во-первых, комплексная терапия обеспечивает синергидный эффект. Во-вторых, позволяет снизить дозу противовирусного химиопрепарата, уменьшая вероятность развития НЛР, сокращая его токсическое воздействие на организм и снижая вероятность возникновения устойчивых штаммов герпес-вирусов. Кроме того, это значительно сокращает продолжительность острого периода болезни и сроки лечения.
Одним из препаратов, показавшим свою эффективность при лечении герпес-ассоциированных заболеваний у детей, является инозин пранобекс. Инозин пранобекс — это синтетическое комплексное производное пурина, обладающее иммуностимулирующей активностью и неспецифическим противовирусным действием. Препарат восстанавливает функции лимфоцитов в условиях иммунодепрессии, повышает бластогенез в популяции моноцитарных клеток, стимулирует экспрессию мембранных рецепторов на поверхности Т-хелперов, оказывает стимулирующее влияние на активность цитотоксических Т-лимфоцитов и естественных киллеров, функции Т-супрессоров и Т-хелперов, повышает продукцию иммуноглобулина G, интерферонов, интерлейкинов (ИЛ-1 и ИЛ-2), снижает образование провоспалительных цитокинов (ИЛ-4 и ИЛ-10), потенцирует хемотаксис нейтрофилов, моноцитов и макрофагов. Механизм противовирусного действия препарата связан с ингибированием вирусной РНК и фермента дигидроптероатсинтетазы, участвующего в репликации, усилении подавленного вирусами синтеза мРНК лимфоцитов, что сопровождается угнетением биосинтеза вирусной РНК и трансляции вирусных белков.
Инозин пранобекс малотоксичен, хорошо переносится, в России рекомендован в виде таблеток детям с 3-летнего возраста (масса тела более 15 кг). За рубежом он доступен и в форме сиропа и не имеет возрастных ограничений. Препарат назначается по 50–100 мг/кг/сут внутрь в 3–4 приема в течение всего острого периода болезни (5–10 дней в зависимости от длительности вирусемии и выраженности синдрома интоксикации). В качестве поддерживающей терапии для восстановления иммунологических показателей возможно назначение препарата по иммуномодулирующей схеме (50 мг 2 раза в день в течение 14–28 дней). Доказана высокая эффективность курсовой терапии инозином пранобексом (50 мг/кг массы тела в сутки в 3–4 приема внутрь, три курса лечения по 10 дней с интервалом 10 дней) [7], комбинированной курсовой терапии с использованием инозина пранобекса и рекомбинантного интерферона α-2β (3 курса по 10 дней с интервалом 14 дней) у детей с микст-вирусными инфекциями [8].
Применение инозина пранобекса как препарата с иммунотропным и противовирусным действием на различных этапах лечебно-профилактических мероприятий позволяет избежать полипрагмазии, тем самым снизить медикаментозную нагрузку на организм и уменьшить риск нежелательных эффектов.
Литература
- Кускова Т. К., Белова Е. Г. Семейство герпес-вирусов на современном этапе // Лечащий Врач. 2004, № 5, с. 64–69.
- Hjalgrim H., Askling J., Rostgaard K. et al. Characteristics of Hodgkin’s lymphoma after infectious mononucleosis // N. Engl. J. Med. 2003; 349: 1324–1332.
- Никольский И. С., Юрченко В. Д., Никольская К. И. Характеристика активной хронической Эпштейна–Барр вирусной инфекции: клинико-иммунологический синдром // Современные инфекции. 2003, № 3, с. 60–62.
- Katz B. Z., Shiraishi Y., Mears C. J., Binns H. J., Taylor R. Chronic fatigue syndrome after infectious mononucleosis in adolescents // Pediatrics. 2009, Jul; 124 (1): 189–193.
- Lerner A. M., Begar S. N., Deeter R. G. IgM serum antibodies to Epstein-Barr virus are uniquely present in a subset of patients with the chronic fatigue syndrome // In Vivo. 2004, Mar-Apr; 18 (2): 101–106.
- Maakaroun N. R., Moanna A., Jacob J. T., Albrecht H. Viral infections associated with haemophagocytic syndrome // Rev. Med. Virol. 2010, Mar; 20 (2): 93–105.
- Симованьян Э. Н., Денисенко В. Б., Григорян А. В. Эффективность применения инозина пранобекс у часто болеющих детей с хронической Эпштейна-Барр вирусной инфекцией: результаты рандомизированного исследования // Вопросы современной педиатрии. 2011, Т. 10, № 2, С. 16–21.
- Нестерова И. В., Ковалева С. В., Чудилова Г. А., Ломтатидзе Л. В., Клещенко Е. И., Шинкарева О. Н. Динамика изменений фенотипа и функциональной активности нейтрофильных гранулоцитов у иммунокомпрометированных детей с повторными ОРВИ, ассоциированными с герпесвирусными инфекциями, на фоне комбинированной интерфероно- и иммунотерапии // Цитокины и воспаление. 2014, Т. 13, № 1, с. 113.
Т. А. Бокова,доктор медицинских наук, профессор
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва
Контактная информация: bta2304@mail.ru
Купить номер с этой статьей в pdf
Источник


