Планшеты ифа для герпеса

На основе рекомбинантного белка gG2 (JSC Diaproph-Med) сконструировано тест-систему для выявления иммуноглобулинов класса G к вирусу герпеса 2 типа и определения индекса их авидности. Данную тест-систему можно использовать как для подтверждения первичной инфекции, так и для дифференциации первичного заболевания от хронического инфекционного процесса и реактивации вируса. Таким образом, разработанная нами тест-система может быть дополнительным методом диагностики герпетической инфекции.
Инфицирование вирусом простого герпеса 2 (ВПГ2) типа является причиной большинства случаев хронического и рецидивирующего генитального герпеса. Для данной инфекции характерны горизонтальный (от больного к здоровому половым путем) и вертикальный (от матери плоду) способы передачи [1].
Несмотря на высокую гомологию с родственным вирусом простого герпеса 1 типа ВПГ2 является более опасным, поскольку характеризуется выраженным тропизмом к эпителиоцитам слизистых оболочек полового тракта и длительная персистенция вируса может приводить к онкогенной трансформации зараженных клеток [2]. Инфекция, обусловленная ВПГ2, характеризуется более частыми рецидивами, в сравнении с ВПГ1-инфекцией, и может быть причинами невынашивания беременности и развития врожденных патологий плода. [3, 4].
Рис. 1. Схематическое строение вируса простого герпеса.
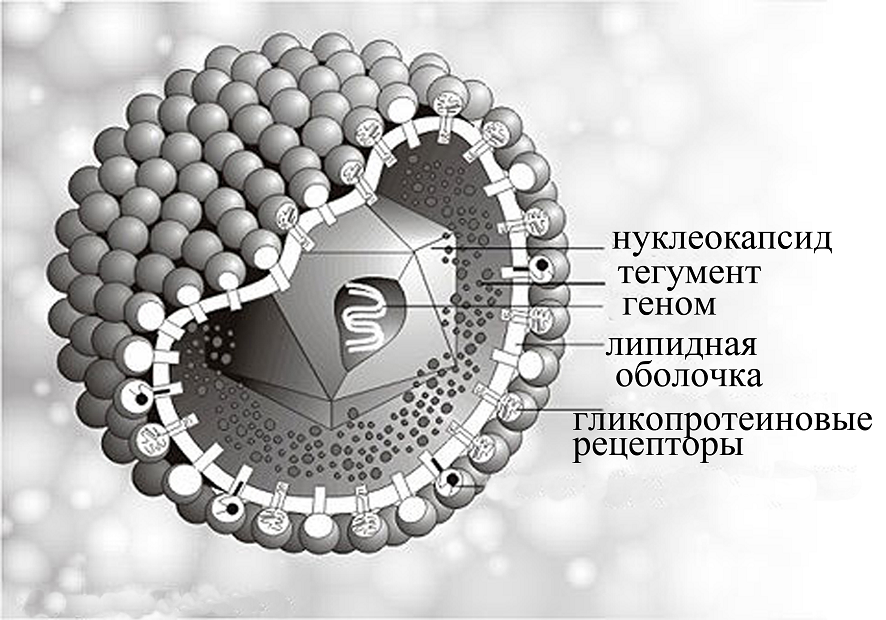
Диагностическое значение при первичном инфицировании ВПГ2 имеют IgM, которые определяются в крови на 4-6 сутки после контакта с вирусом и достигают максимального значения на 15-20 сутки. С 10-14 суток начинается продукция специфических IgG, которые персистируют в органихме на протяжении всей жизни [5]. Поэтому, серологические методы позволяют диагностировать заболевание как в период активации вируса, так и во время латентной инфекции. Антитела класса М к ВПГ2 выявляются в организме не только при первичной инфекции, но также и при реактивации вируса и реинфекции. В связи с этим, при установлении факта первичного инфицирования обязательным является определение авидности специфичесикх антител класса G [6, 7].
Рис. 2. Развитие иммунного ответа при герпетической инфекции
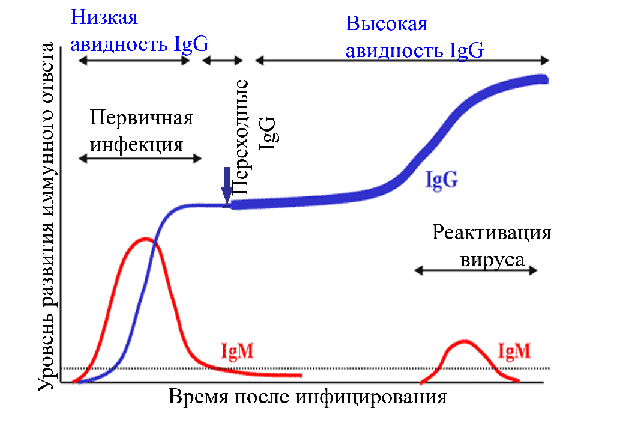
Авидность – это показатель сродства активного центра антитела к антигенным детерминантам возбудителя, который пропорционален степени прочности иммунного комплекса. Высокоаффинные антитела имеют преимущество в реакции антиген-антитело благодаря формированию к более устойчивых связей, что обусловлено эффективными конформационными изменениями их активных центров.
Антитела с высоким индексом авидности формируют высокоэнергетические иммунные комплексы с низкой тенденцией к диссоциации, и наоборот, антитела с низким индексом авидности образуют комплексы, для диссоциации которых необходимо меньше энергии. На этом свойстве базируется метод определения индекса авидности антител в присутствии хаотропных агентов (мочевина, гуанидина гидрохлорид, изотиоцианат натрия), низкие концентрации которых препятствуют возникновению иммунных комплексов, в состав которых входят только низкоавидные антитела.
Специфические IgG с низкой авидностью определяются тлько на ранних этапах первичной герпетической инфекции, что и даёт возможность дифференцировать ёё от хронического рецидивирующего заболевания [8].
Перспективным направлением в серодиагностике ВПГ2 является разработка различных конструкций твердофазного ИФА. Использование типоспецифического рекомбинантного белка gG2 даёт возможность дифференцировать герпетическую инфекцию, вызванную ВПГ2, от заболеваний вызванных подобным вирусом ВПГ1, что имеет существенное прогностическое значение и определяет дальнейшую стратегию лечения. [7, 9].
Материалы и методы
Исследовали 510 образцов сывороток крови доноров, переданных областной станцией переливания крови Киевской области. Все образцы были подтверждены в тест-системе «AMERICA Herpes 2 IgG Antibody ELISA Test Kit» (IBL, США).
Иммуноферментная тест-система для определения иммуноглобулинов класса G была сконструирована в формате непрямого твердофазного ИФА.
Для приготовления иммуносорбента использовали 96-луночные планшеты PolySorp (NUNC, Дания), лунки которого были очищенным рекомбнантным белком gG2 HSV2 производства ЧАО НПК «Диапроф Мед» (Киев, Украина).
Данный рекомбинантный белок gG2, состоящий из 68 аминокислот, является антигенным аналогом иммунодоминантных участков поверхностного гликопротеина G ВПГ2. При конструировании продуцента рекомбинантного белка использовали плазмидный вектор pET28а (Novagen, США) и клеточную систему реципиентного штамма Esherichia coli BL21(DE3).
Постановку ИФА проводили двухэтапно. На первом этапе, при внесении в лунки планшета исследуемых сывороток, содержащиеся в них специфические антитела связывались с соответствующими антигенами иммуносорбента. На следующем этапе образованные иммунные комплексы выявляли с помощью пероксидазного конъюгата на основе мышиных моноклональных антител к IgG человека.
В качестве проявителя реакции использовали 0,03% раствор 3,3’,5,5’- тетраметилбензидина в цитратном буфере, который содержал 0,016% перекиси водорода (субстрат для фермента пероксидазы). Развитие цветной реакции останавливали 0,5М серной кислотой. Оптическую плотность реакционной смеси в лунках определяли спектрофотометром Labsystems Multiskan (Финляндия) в двухволновом режиме 492/620 нм. Результат считали положительным, если его оптическая плотность (ОП) превышала граничное значение (cut off), которое рассчитывали как сумму среднего значения трёх негативных контролей с учетом коэффициента 0,2.
В качестве негативного контроля использовали сыворотку крови человека, которая не содержала антител к ВПГ1, ВПГ2, вирусу гепатита С, T.pallidum, а также HBsAg вируса гепатита В.
Для определения индекса авидности исследуемую положительную сыворотку инкубировали в двух параллельных лунках иммуносорбента, потом одну из них промывали в обычном режиме, а другую обрабатывали диссоциирующим раствором, который приводит к разрушению иммунных комплексов, образованных низкоавидными антителами. Индекс авидности рассчитывали как соотношение оптической плотности, полученной при выявлении специфических антител в присутствии диссоциирующего агента, к оптической плотности, полученной в результате анализа данного образца без обработки диссоциирующим раствором.
Если индекс авидности был меньше 30% считали, что сыворока содержит низкоавидные антитела; больше 60% — высокоавидные; а в диапазоне от 30% до 60% — средний уровень авидности антител.
Для разведения исследуемых образцов и конъюгата использовали фосфатный буфер с добавлением белка казеиновой фракции молока и детергента Tween 20 в качестве компонентов, которые блокируют неспецифические сигналы.
Для промывания планшетов после каждого этапа использовали фосфатный буфер с добавлением детергента Triton-X100.
Каждую сыворотку тестировали в четырёх повторах. Обработку полученных результатов проводили с учётом критерия Стьюдента [11].
Результаты и обсуждение
Для определения качественных характеристик разработанной нами тест-системы, предназначенной для определения IgG к ВПГ2, было исследовано 510 сывороток крови доноров. Полученные результаты представлены на рис.3.
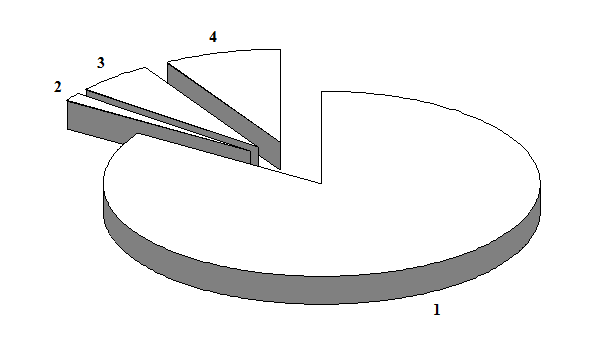
Рис.3. Распределение антител класса G, специфичных к ВПГ2, среди доноров: 1 – количество сывороток, не содержащих антитела к ВПГ2; 2 – количество сывороток, содержащих специфичные антитела с низким индексом авидности; 3 – количество сывороток, содержащих специфичные антитела со средним индексом авидности; 4 – количество сывороток, содержащих специфичные антитела с высоким индексом авидности.
Среди проанализированных образцов в 96 (18,8%) сыворотках выявлены специфические антитела класса G, а остальные 414 (81,2%) – были серонегативными. Такие данные соответствуют распространённости вируса в странах восточной Европы [12].
Определение индекса авидности специфических IgG основывается на способности связи антиген-антитело разрушаться под воздействием диссоциирующего раствора. Прочность иммунного комплекса определяется степенью сродства активного центра антитела с антигенными детерминантами вируса, что зависит от длительности и продуктивности заболевания.
При тестировании доноров с помощью разработанной тест-системы в наших исследованиях антитела класса G с низким индексом авидности — до 30% были выявлены у 8 серопозитивних доноров. Это свидетельствует о первичном инфицировании ВПГ2, поскольку контакт с вирусом состоялся сравнительно недавно и активные центры антител в процессе иммунного ответа еще не приобрели высокой степени сродства к антигену.
Специфические IgG с высоким индексом авидности – более 30% — были выявлены у 88 серопозитивных доноров (91,7%), что указывает на инфекцию, перенесённую ранее. В пределах этой группы можно выделить подгруппу из 53 доноров (55,2%), у которых индекс авидности составлял 60-100%. Такие данные могут свидетельствовать о поздней стадии перенесённой первичной инфекции или инфекции, перенесённой в прошлом. Средний индекс авидности в интервале 30-60%, который наблюдается у 35 доноров (36%), можно рассматривать как переходной этап развития иммунного ответа, а именно, процесс формирования специфичности активного центра антител [13]. Известно, что динамика авидности иммуноглобулинов зависит от дозы антигена. При низкой вирусной нагрузке происходит более быстрое нарастание авидности, а большое количество вируса приводит к более медленному формированию авидности [14].
Таким образом, низкоавидные антитела продуцируются в течении первой стадии инфекции, когда содержание вирусных антигенов высокое. Также следует обратить внимание, что длительность периода циркуляции в организме низко- и среднеавидных антител может быть обусловлен индивидуальными особенностями функционирования иммунной системы. Поэтому окончательный вывод и интерпретацию полученных результатов можно сформулировать только после исследования динамики количества и индекса авидности антител, специфических к ВПГ2.
Таким образом, разработанная нами тест-система для определения антител к ВПГ2 с определением индекса их авидности даёт возможность устанавливать длительность и стадию инфекционного процесса, что может оказаться решающим фактором при выборе стратегии лечения.
Литература
- Марієвський В.Ф., Руденко А.О., Щербинська А.М. Инфекционные болезни в Украине на рубеже двух столетий. //Современные инфекции.-1999.-№2.-С.18-23.
- Кицак В.Я. Вирусные инфекции беременных: патология плода и новорожденных. – Кольцово, 2005. – 84 с.
- Казимирчук В.Е., Мальцев Д.В. Клиника, диагностика и лечение герпесвирусных инфекций человека. – К.: Феникс, 2009. – 352 с.
- Leyland B., Kennedy M.R., Wimberly Y.H., Levine B.J., Cherpes T.L. Serologic detection of herpes simplex virus type 2 antibodies among pregnant women using a point-of-care test from Focus Diagnostics. // Journal of Clinical Virology. – 2009. – Vol. 44, № 2. — P. 125-128.
- Slomka M.J. Seroepidemiology and control of genital herpes: the value of type specific antibodies to herpes simplex virus. // Commun Dis Rep CDR Rev. – 1996. – Vol. 1, №6(3). — Р. 41-45.
- Brown E.L., Morrow R., Krantz E.M. at all. Maternal herpes simplex virus antibody avidity and risk of neonatal herpes. // Am J Obstet Gynecol. – 2006. — Jul;195(1). – P. 4-6.
- Morrow R.A., Friedrich D., Krantz E., Wald A. Development and use of a type-specific antibody avidity test based on herpes simplex virus type 2 glycoprotein G. // Sex Transm Dis. – 2004. — Aug;31(8). – P. 508-515.
- Hashido M., Inouye S., Kawana T. Differentiation of primary from nonprimary genital herpes infections by a herpes simplex virus-specific immunoglobulin G avidity assay. // Journal of Clinical Microbiology. – 1997. – Vol. 35, № 7. – Р.1766-1768.
- Manservigi R., Cassai E. The glycoproteins of the human herpesviruses. // Comparative Immunology, Microbiology and Infectious Diseases. – 1991. – Vol. 14, № 2 — P. 81-95.
- Tijssen P., Kustak E. Higly efficient and simle metods for the preparation of peroxidase and active peroxidase antibody conjuigates for enzyme immunoassays // Analytical Biochemistry. – 1984. – Vol. 136, № 2. — Р. 451-457.
- Лапач С.Н., Губенко А.В., Бабич П.Н. Статистические методы в медико-биологических исследованиях с использованием Excel – К.: Морион, 2001. — 407с.
- Corey L. Challenges in genital herpes simplex virus management. // The Journal of Infectious Diseases. – 2002. – Vol. 15;186 Suppl 1. – P. 29-33.
- Скок М.В. Основи імунології. Курс лекцій – Київ: Фітосоціоцентр, 2002. – 152с.
- Meyers R.A. Immunology: from cell biology to disease. — Wiley-VCH, 2007. – 435р.
Источник

БиоСкрин-ВПГ
2.784,00 руб.
![]()
БиоСкрин-ВПГ (# E-0644)
Количество тестов: 64
Срок годности: 12 месяцев
Хранение: 2-8°C
Продолжительность анализа: <3 часов
Набор реагентов предназначен только для научных исследований!
Инструкция
Набор реагентов основан на принципе непрямого иммуноферментного анализа и предназначена для:
— определения вирусоспецифических антител при сероэпидемиологических исследованиях;
— выявления серонегативных лиц в группах риска (например, у лиц с иммунодефицитами);
— определения иммунного статуса в отношении вируса герпеса;
— отбора плазмы с повышенным содержанием антител к вирусу герпеса при производстве иммуноглобулинов;
— диагностики первичной герпетической инфекции (при наличии парных сывороток).
Параллельное исследование сыворотки в лунках с вирусным и контрольным антигенами позволяет исключить получение ложноположительных результатов.
__________________________________________________________________________________________________________________________________________

БиоПрайм-ВПГ
3.630,00 руб.
![]()
БиоПрайм-ВПГ (# E-0663)
Количество тестов: 48
Срок годности: 12 месяцев
Хранение: 2-8°C
Продолжительность инкубаций: 2 часа
Регистрационное удостоверение: № РЗН 2013/672
Инструкция
Набор реагентов «БиоПрайм-ВПГ» предназначен для определения индекса авидности (см. инструкцию) специфических иммуноглобулинов класса G к вирусу простого герпеса 1 и 2 типа и для диагностики первичной герпесвирусной инфекции. Принцип метода основан на выявлении «ранних» низкоавидных иммуноглобулинов класса G. Наличие низкоавидных антител является индикатором первичной инфекции в предшествующие 2-3 месяца. Метод является альтернативным методу выявления вирусоспецифических антител класса М и не требует наличия парных сывороток для постановки диагноза.
Для определения индекса авидности антител IgG каждый образец сыворотки или плазмы крови человека исследуют методом иммуноферментного анализа в двух параллельных лунках планшетов с иммобилизованными антигенами вируса герпеса. При этом антитела, специфичные к белкам ВПГ человека, взаимодействуют с адсорбированными антигенами, образуя иммунные комплексы.
После инкубации с исследуемой сывороткой опытные лунки дополнительно обрабатывается денатурирующим раствором, избирательно разрушающим образовавшиеся комплексы низкоавидных антител с антигеном, но не влияющим на комплексы с высокоавидными антителами. На присутствие в исследуемом образце низкоавидных антител указывает снижение оптического поглощения в лунке, обработанной денатурирующим раствором, в сравнении с контрольной лункой.
________________________________________________________________________________________________________________________________________________

БиоСет-актив-ВПГ
4.664,00 руб.
![]()
БиоСет-актив-ВПГ (# Е-0672)
Количество тестов: 32
Срок годности: 12 месяцев
Хранение: 2-8°C
Продолжительность инкубаций: 1 час 15 минут
Регистрационное удостоверение: № РЗН 2013/670
Инструкция
Набор реагентов предназначен для выявления антител к ДНК-связывающим белкам ВПГ-1 и ВПГ-2 в активной стадии герпетической инфекции в сыворотке или плазме крови человека методом иммуноферментного анализа.
Источник
Описание
ИФА-ВПГ IgG
ИФА-ВПГ IgG № ФСР 2011/11263 от 07.07.2011
Тест-система иммуноферментная для выявления антител класса G к вирусу простого герпеса 1 типа
И Н С Т Р У К Ц И Я
по применению набора реагентов
«ИФА-ВПГ-2-IgG»
Тест-система иммуноферментная для выявления
иммуноглобулинов класса G к вирусу простого герпеса II типа
Регистрационное удостоверение №ФСР 2009/06108 от «25»ноября 2009 г.
НАЗНАЧЕНИЕ
Выявление и определение титра видоспецифических иммуноглобулинов класса G к вирусу простого герпеса II типа (ВПГ-2) в сыворотке (плазме) крови человека методом непрямого иммуноферментного анализа (ИФА) на твердофазном носителе при «ручной» постановке и с использованием ИФА-анализаторов.
СОСТАВ И КОМПЛЕКТАЦИЯ НАБОРА
| Иммуносорбент | лизатный инактивированный очищенный антиген вируса простого герпеса II типа (ВПГ-2), сорбированный на 96-луночном разборном полистироловом планшете для иммунологических реакций с плоским дном (используются «ломающиеся» стрипы) | 1 планшет |
| допускается раздельная упаковка стрипов (по 1-4 стрипа в пакете) | ||
| Контрольный положительный образец (К+) | инактивированный; содержит антитела класса G к ВПГ-2 в титре 1:500; прозрачная красного цвета жидкость | 1 фл. (1,2 мл) |
| Контрольный образец уровня «среза» (К+пор) | инактивированный; содержит антитела класса G к ВПГ-2 в «пороговом» титре (1:100); прозрачная желтого цвета жидкость | 1 фл. (1,2 мл) |
| Контрольный отрицательный образец (К–) | инактивированный; прозрачная зеленого цвета жидкость | 1 фл. (1,2 мл) |
| Конъюгат | антитела моноклональные мышиные против иммуноглобулинов человека класса G, меченые пероксидазой хрена; прозрачная розового цвета жидкость | 1 фл. (13 мл) |
| Раствор индикаторный (РИ) | стабилизированный раствор тетраметилбензидина; прозрачная бесцветная или светло-желтая жидкость | 1 фл. (13 мл) |
| 25-кратный концентрат фосфатно-солевого буферного раствора с твином [ФСБ-Т(х25)] | прозрачная или слегка опалесцирующая пенящаяся бесцветная жидкость; возможно выпадение осадка солей белого цвета, растворяющегося при температуре 37 0С в течение 30 мин | 1 фл. (80 мл) или 2 фл. (по 40 мл) |
| Раствор для разведения образцов (РРО) | прозрачная жидкость синего цвета | 1 фл. (15 мл) |
| Раствор для предварительного разведения образцов (РПРО) | прозрачная жидкость розового цвета | 1 фл. (по 15 мл) |
| Стоп-реагент | прозрачная бесцветная жидкость | 1 фл. (12,5 мл) |
Примечания. 1. Набор включает все реагенты, необходимые для постановки ИФА, кроме очищенной (дистиллированной или деионизированной) воды.
- ФСБ-Т(х25), РИ,РРО,РПРО, стоп-реагент – унифицированы для всех наборов ЗАО «ЭКОлаб», в которых используются указанные реагенты.
Набор может быть дополнительно укомплектован:
вспомогательным планшетом для разведения образцов (1 шт.),
вспомогательными пластиковыми емкостями (4 шт.),
одноразовыми наконечниками для автоматических пипеток (16 шт.)
клейкой пленкой для планшетов (4 шт.).
Компоненты набора упакованы в коробку, в коробку вложена инструкция по применению и бланк калибровочного графика.
По желанию потребителя базовая комплектация набора (число индивидуальных упаковок с реагентами и их объемы) может быть изменена.
ОСНОВНЫЕ ПОТРЕБИТЕЛЬСКИЕ ХАРАКТЕРИСТИКИ
Базовый вариант комплектации набора позволяет одномоментное исследование 96 образцов, включая контрольные (на контрольные образцы используется 6 лунок, одна лунка – для выведения уровня «бланк»). Предусмотрена возможность проведения раздельных исследований с использованием необходимого количества стрипов:
| Число стрипов | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| Число иссл. обр. | 1 | 2-9 | 10-17 | 18-25 | 26-33 | 34-41 | 42-49 | 50-57 | 58-65 | 66-73 | 74-81 | 82-89 |
ПРИНЦИП МЕТОДА
При наличии в исследуемом образце иммуноглобулинов класса G к ВПГ-2 они во время первой инкубации связываются с антигеном ВПГ-2, сорбированным на поверхности лунок полистиролового планшета. Этот комплекс во время второй инкубации связывается с конъюгатом – антителами против IgG человека, меченными пероксидазой хрена. Далее, после добавления индикаторного раствора (хромоген — тетраметилбензидин) в результате ферментативной реакции реакционная смесь в лунках планшета окрашивается пропорционально концентрации антител класса G к ВПГ-2. Реакция останавливается добавлением стоп-реагента. Интенсивность окрашивания (оптическая плотность) регистрируется с помощью спектрофотометра.
АНАЛИТИЧЕСКИЕ И ДИАГНОСТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
Диагностическая чувствительность и диагностическая специфичность при проверке на сыворотках стандартизованной панели предприятия или аналогичных коммерческих панелей, разрешенных к применению в РФ – 100 %.
ИССЛЕДУЕМЫЕ ОБРАЗЦЫ
Сыворотка (плазма) крови человека объемом не менее 10 мкл.
Образцы до исследования можно хранить не более 7 сут при температуре от 2 до 8 оС или до 3 мес при температуре минус 20 оС или более низкой. Допускается только однократное замораживание-размораживание образцов. Размороженные образцы перед исследованием тщательно перемешать.
Не допускается использование для исследования образцов с повышенным содержанием липидов и (или) с признаками гемолиза, и (или) с видимым микробным проростом.
Образцы, содержащие осадок, перед анализом отцентрифугировать в течение 10-15 мин при 2500-3000 об/мин.
МЕРЫ ПРЕДОСТОРОЖНОСТИ
Набор биологически безопасен, однако образцы сывороток крови человека следует рассматривать как потенциально инфицированные.
Стоп-реагент при попадании на незащищенную кожу и слизистые может вызывать химические ожоги. В случае попадания на кожу – немедленно промойте пораженный участок водой.
СПОСОБ ПРИМЕНЕНИЯ
Оборудование и материалы (для «ручной» постановки)
Дозаторы пипеточные (пипетки полуавтоматические одно- и многоканальные переменного объема) для внесения реагентов в лунки планшета с погрешностью дозирования не более 5 % с наконечниками полипропиленовыми одноразовыми.
Ручные, или автоматические промыватели, или восьми- и двенадцатиканальные пипеточные дозаторы для промывания лунок планшета.
Спектрофотометр вертикального сканирования для измерения оптической плотности в лунках планшета при 450 нм и/или в двухволновом режиме при основной длине волны 450 нм и длине волны сравнения в диапазоне 620-650 нм.
Центрифуга лабораторная на 2,5-3,0 тыс. об/мин, термостат на 37 оС, холодильник бытовой, фильтровальная бумага.
Вода очищенная (дистиллированная или деионизированная).
70 %-ный раствор спирта этилового и 6 %-ный раствор перекиси водорода (дез.растворы) или растворы иных дезинфектантов, разрешенных к применению СП 1.32322-08, кроме хлорсодержащих.
Приготовление рабочих растворов реагентов для ИФА
Перед работой извлечь набор из холодильника, вскрыть упаковку и выдержать все реагенты перед проведением анализа не менее 30 мин при температуре от 18 до 25 оС.
Предварительное разведение исследуемых образцов
Исследуемые образцы развести 1:10 во вспомогательном планшете. Для этого внести в его лунки по 90 мкл РПРО и добавить по 10 мкл сыворотки, тщательно перемешать пипетированием. При этом розовый цвет должен измениться на желтый. Если изменение цвета не произошло, данный образец необходимо исследовать повторно с целью исключения неправильных результатов. Рабочее разведение (1:100) готовить непосредственно в лунках иммуносорбента (см. раздел Проведение ИФА («ручная» постановка), п. 2).
Рабочие разведения образцов хранить не более 6 ч при температуре от 18 до 25 оС.
Приготовление рабочего промывочного раствора (ФСБ-Т)
При выпадении осадка солей в ФСБ-Т(х25) прогреть его при температуре 37 оС до полного растворения осадка.
При постановках с использованием ИФА-анализаторов 80 мл ФСБ-Т(х25) довести водой очищенной до 2 л.
При дробной «ручной» постановке использовать соотношения объемов ФСБ-Т(х25) и воды, указанные в табл. 1 для разного числа используемых стрипов.
Таблица 1
| Число стрипов | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| ФСБ-Т(х25), мл | 7 | 10 | 13 | 17 | 20 | 23 | 27 | 30 | 33 | 37 | 40 |
| Вода очищенная, мл | до 175 | до 250 | до 325 | до 425 | до 500 | до 575 | до 675 | до 750 | до 825 | до 925 | до 1000 |
Готовый рабочий промывочный раствор хранить при температуре от 2 до 8 ºС не более 14 сут.
Приготовление остальных реагентов
К–, К+, К+пор, конъюгат, РИ,РРО,РПРО, и стоп-реагент готовы к применению.
После вскрытия упаковок неиспользованные реагенты допускается хранить в плотно закрытых упаковках при температуре от 2 до 8 оС до истечения срока годности.
Проведение ИФА («ручная» постановка)
Внимание! Соблюдение указанных ниже температуры и времени инкубации планшетов на каждой стадии постановки крайне важно для получения достоверных результатов.
- Извлечь из упаковки рамку планшета и необходимое число стрипов. Неиспользованные стрипы допускается хранить в плотно закрытом пакете с влагопоглотителем при температуре от 2 до 8 оС до истечения срока годности.
- В лунку А1 внести 100 мкл РРО, в следующие лунки внести по 100 мкл контрольных образцов (по 2 лунки на образец), оставшиеся лунки использовать для исследуемых образцов (по 1 лунке на образец), для чего внести в них: вначале по 90 мкл РРО, а затем – по 10 мкл образцов, предварительно разведенных 1:10 в лунках вспомогательного планшета (см. раздел «Предварительное разведение исследуемых образцов»), тщательно перемешать пипетированием.
- Планшет закрыть крышкой или клейкой пленкой. Инкубировать планшет 30 минут при температуре от 21 до 250С в защищенном от света месте.
- С помощью промывателя удалить содержимое лунок, 4 раза промыть планшет промывочным раствором, внося в лунки 350-370 мкл раствора. При наличии промывателя, позволяющего производить промывку в режиме «Overflow», использовать именно этот режим. По окончании промывки остатки раствора удалить из лунок, постукивая перевернутым планшетом по сложенной в несколько слоев фильтровальной бумаге.
- Во все лунки внести по 100 мкл конъюгата
- Планшет закрыть крышкой или клейкой пленкой., инкубировать 30 минут при температуре от 21 до 250С в защищенном от света месте.
- С помощью промывателя удалить содержимое лунок, 4 раза промыть планшет как указано в п. 4.
- Во все лунки внести по 100 мкл раствора индикаторного, немедленно поместить планшет в защищенное от света место и инкубировать 10–15 минут при температуре от 21 до 250С.
- Внести во все лунки в той же последовательности, как и раствор индикаторный, по 100 мкл стоп-реагента, осторожно (постукиванием по планшету) перемешать содержимое лунок и не более чем через 10 мин приступить к учету результатов.
Регистрация и учет результатов качественного исследования
Результаты ИФА регистрировать спектрофотометрически, выводя спектрофотометр на нулевой уровень («бланк») по лунке А1 и измеряя оптическую плотность (ОП) при двух длинах волн – 450 нм и 620-650 нм. При отсутствии референс-фильтра на 620-650 нм оптическую плотность (ОП) измерять при длине волны 450 нм.
Результаты ИФА учитывать при следующих условиях:
среднее значение ОПК+ – не менее 0,60;
среднее значение ОПК+пор – не менее 0,20;
отношение среднего значения ОПК+ к среднему значению ОПК+пор – не менее 1,5;
среднее значение ОПК– – не более 0,10.
В противном случае исследование необходимо повторить.
Полученные результаты считать:
- положительными, если ОПобразца больше 1,1×ОПК+пор ;
- отрицательными, если ОПобразца меньше 0,9×ОПК+пор ;
- сомнительными, если ОПобразца = (1+0,1)×ОПК+пор.
При получении сомнительных результатов сыворотки рекомендуется исследовать повторно в двух лунках тест-системы. Если результаты опять попадут в пределы сомнительных, следует провести тестирование сывороток, отобранных через 2-4 недели. Если и в данном случае результаты попадут в пределы сомнительных, образцы сывороток считать отрицательными.
Определение титра антител
Для определения титра антител класса G к ВПГ-2 на стандартном бланке (входит в состав набора) строится калибровочный график. Для этого по оси абцисс (логарифмическая шкала) откладываются значения титров К+ (1:500) и К+пор (1:100), а по оси ординат (пропорциональная шкала) – соответствующие им средние значения ОП, полученные в ИФА. Полученные точки соединяются прямой линией. Титр антител в исследуемом образцах определяется по калибровочному графику как абсцисса точки, ордината которой равна полученному в ИФА значению ОП.
Если ОПобразца превышает ОПК+, для более точного определения титра рекомендуется при повторном анализе развести данный образец дополнительно. Повторить анализ и полученное по графику значение титра увеличить соответственно дополнительному разведению.
ПОСТАНОВКА С ИСПОЛЬЗОВАНИЕМ ИФА-АНАЛИЗАТОРОВ
Подготовить прибор в соответствии с инструкцией по его эксплуатации, ввести программу анализа, соответствующую используемому набору, и провести анализ.
СРОК ГОДНОСТИ
Срок годности набора – 1 год. Набор с истекшим сроком годности применению не подлежит.
ХРАНЕНИЕ И ТРАНСПОРТИРОВАНИЕ
Хранение
В упаковке предприятия-изготовителя при температуре от 2 оС до 8 оС. Замораживание не допускается.
Транспортирование
При температуре от 2 оС до 8 оС. Замораживание не допускается. Допускается транспортирование при температуре от 9 оС до 25 оС в течение 10 сут.
УСЛОВИЯ ОТПУСКА
Для учреждений здравоохранения.
По вопросам, касающимся качества набора, следует обращаться по адресу 142530, Московская обл., г. Электрогорск, ул. Буденного,a д.1, ЗАО «ЭКОлаб» тел: (49643)3-1374, 3-2311, факс 3-3143, и в учреждение, уполномоченное на проведение Государственного контроля указанной продукции.
КРАТКАЯ СХЕМА ИФА
(ИФА-ВПГ-2-IgG)
Использовать только после тщательного ознакомления с инструкцией!
| Внести | в лунку А1– 100 мкл РРО, в лунки B1, С1-. по 100 мкл К+, в лунки D1, E1-по 100 мкл К+пор в лунки F1,G1 –по 100 мкл К-, в остальные лунки – вначале по 90 мкл РРО, а затем – по 10 мкл образцов, предварительно разведенных 1:10 в лунках вспомогательного планшета (см. раздел «Предварительное разведение исследуемых образцов») |
| Инкубация | 30 мин, 21-25 оС |
| Промыть | 4 раза промывочным раствором |
| Внести | по 100 мкл конъюгата в каждую лунку |
| Инкубация | 30 мин, 21-25 оС |
| Промыть | 4 раза промывочным раствором |
| Внести | по 100 мкл индикаторного раствора в каждую лунку |
| Инкубация | 10-15 мин, 21-25 оС |
| Внести | по 100 мкл стоп-реагента в каждую лунку |
| Измерить | ОП при 450 нм (референс 620-650 нм), «бланк» — по лунке А1 |
Скачать Инструкцию
Скачать РУ
Источник


