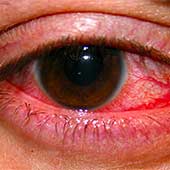
Доказательная медицина лечение герпеса
На сегодняшний день известно более 8 типов герпес-вирусов человека. Наиболее актуальны первые 6 типов. Для всех вирусов этой группы характерен сходный инфекционный процесс: при инфицировании ранее не болевшего человека происходит первичная инфекция, она может проявляться в манифестной форме (с выраженными клиническими симптомами), а так же в латентной (стертой) или бессимптомной форме, что можно определить лишь впоследствии по появлению специфических антител.
После первичного инфицирования герпес-вирус остается в организме пожизненно, в «неактивном» состоянии, что также можно назвать латентной или персистирующей инфекцией. При первичной инфекции организм вырабатывает специфические иммуноглобулины класса IgM, которые уходят при стихании первичной инфекции и более никогда не должны появляться. Чуть позже вырабатываются специфические иммуноглобулины IgG, которые остаются на всю жизнь, и их титр может меняться на протяжении жизни.
В редких случаях, в основном при тяжелых иммунодефицитных состояниях может происходить реактивация инфекции и появление симптомов заболевания. В данном случае происходит значительное нарастание титра специфических антител IgG, но иммуноглобулины класса IgM появляться не должны. Их появление в большинстве случаев свидетельствует о несовершенстве метода исследования (чаще всего это иммунофермпентный анализ – ИФА, особенно производимый вручную), и все спорные анализы необходимо проверять референс-методами , например иммуноблотом или ХЛИА.
Вирусы герпеса 1 и 2 типов (Herpes simplex)
Первичная инфекция протекает в виде известной всем «простуды» — болезненных пузырьковых высыпаний на губах, области носа, или в области гениталий, сопровождающихся жжением и зудом.
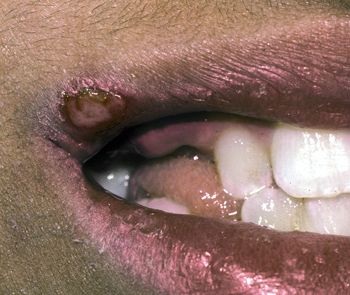
Инфекция склонна к самоизлечению. Для ускорения излечения можно использовать препараты группы ацикловира системно.
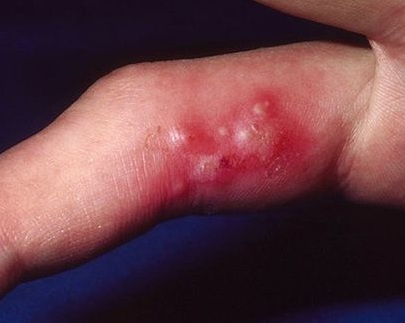
Для данных вирусов характерны частые реактивакции и рецидивы, что в некоторых случаях является показанием для длительного приема противовирусных препаратов группы ацикловира – супрессивной терапии.
Вирусы опасны для плода и новорожденного в случае, если мать до беременности не перенесла первичную инфекцию и не имела антител класса IgG. Инфицирование беременной, не имеющей антител, на ранних сроках может привести к порокам развития плода, а на поздних — к тяжелым заболеваниям новорожденного – герпетическому менингоэнцефалиту.
Вирус герпеса 3 типа – Varicella-Zoster
Первичная инфекция протекает в виде типичной детской инфекции – ветряной оспы. Реактивация вируса протекает в виде «опоясывающего лишая» (Herpes zoster, герпес зостер).
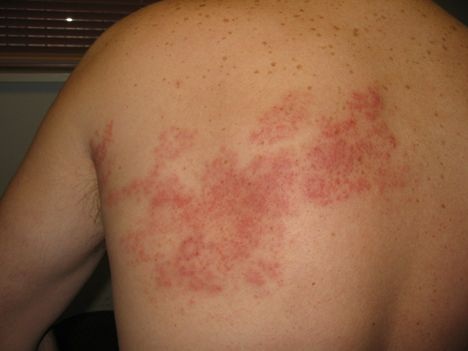
Для профилактики инфекции начиная с детского возраста доступна вакцинация, кроме того, вакцинация контактных с больным ветряной оспой в первые 24-48 часов в подавляющем большинстве случаев предотвращает развитие заболевания.
При развитии заболевания всем взрослым и детям старше 14 лет показано применение противовирусных препаратов группы ацикловира. Лечение ускоряет выздоровление, и предупреждает осложнения инфекции (ветряночный энцефалит, церебеллит). Реактивация инфекции довольно часто встречается у пожилых, снижает качество жизни, может быть причиной хронических болевых синдромов и требует лечения противовирусными препаратами группы ацикловира.
Вирус герпеса 4 типа, или вирус Эпштейна-Барр
Возможны различные варианты первичной инфекции – от латентных, определяемых только по появленю антител, до типичного инфекционного мононуклеоза, у детей первых 3-5 лет первичная инфекция часто протекает в виде затяжной респираторной инфекции, с длительной лихорадкой, иногда с тонзиллитом (ангиной), аденоидитом, увеличение многих групп лимфатических узлов.
В некоторых случаях заболевание затягивается на несколько месяцев, субфебрильная температура и увеличенные лимфатические узлы могут сохраняться до года. У более старший детей, подростков и взрослых заболевание протекает в виде инфекционного мононуклеоза – с высокой лихорадкой, тонзиллофарингитом (ангиной) с выраженным болевым синдромом, аденоидитом иногда с полным отсутствием носового дыхания, увеличением многих групп лимфатических узлов, печени и селезенки. Заболевание протекает доброкачественно, специфической противовирусной терапии не требует и саморазрешается с течением времени.
К вирусу Эпштейна-Барр (ВЭБ) для подтверждения диагноза определяют 4 класса антител:
- IgM VCA – антитела класса IgMк капсидному белку вируса, появляются с первой недели первичной инфекции, далее постепенно уходят. В некоторых случаях могут сохраняться до полугода. Далее никогда появляться не должны.
- IgG VCA – антитела класса IgG появляются в период выздоровления и сохраняются в различных титрах всю жизнь.
- IgG EA – антитела к раннему антигену- появляются в фазу первичной инфекции, немного позднее IgM VCA, далее уходят в течение нескольких месяцев. Их повторное появление свидетельствует о реактивации инфекции.
- IgG EBNA (NA) антитела к ядерному антигену появляются в среднем через 6 месяцев после первичной инфекции и остаются на всю жизнь.
| IgM VCA | IgG EA | IgG VCA | IgG EBNA | |
Нет инфицирования | — | — | — | — |
Первичная инфекция | ++ | +/- | — | — |
Ранняя паст-инфекция (период ранней реконвалесценции) | — | +/- | + | — |
Поздняя паст-инфекция (хроническое носительство) | — | — | + | + |
реактивация | — | + | + | ++ |
Так же вирус можно обнаружить в крови при острой инфекции методом ПЦР. После перенесенной первичной инфекции вирус пожизненно находится в организме и периодически выделяется во внешнюю среду, и может быть обнаружен в различных секретах с помощью ПЦР.
Инфекция, вызванная ВЭБ – самопроходящее заболевание, специфической противовирусной терапии не разработано.
По поводу онкогенности – доказана связь вируса с развитием некоторых лимфом, НО, у лиц о определенной генетической предрасположенностью, в основном у коренного населения Африки.
Вирус герпеса 5 типа, или цитомегаловирус
По аналогии с вирусом Эпштейна-Барр, возможны различные варианты протекания первичной инфекции. Большинство инфицируется цитомегаловирусом в детском возрасте, и у большей части детей первичная инфекция протекает в виде затяжной респираторной инфекции, иногда стерто, в виде длительного субфебрилитета сопровождающегося увеличением лимфатических узлов, иногда – бессимптомно, что выявляется только по появлению специфических антител постфактум. У некоторых – в виде типичного синдрома мононуклеоза, с тонзиллитом, аденоидитом, увеличением печени, селезенки и лимфатических узлов. Иногда заболевание протекает в виде гепатита. Течение первичной инфекции доброкачественное, и в специфическое противовирусной терапии не нуждается.
Цитомегаловирусная инфекция опасна и требует специфической терапии у следующих групп пациентов:
- Лица с ВИЧ инфекцией
- первичными иммунодефицитами
- получающие агрессивную иммуносупрессивную терапию (аутоиммунные заболевания, трансплантация органов).
Так же в отдельных случаях ЦМВ может вызывать инфекцию у новорожденных, рожденных от матерей, не болевших ранее и не имеющих антител класса IgG к ЦМВ. При наличии клинических признаков ЦМВ-инфекции у новорожденного в первые недели жизни (гепатит, пневмонит, поражение ЦНС в виде менингоэнцефалита), хориоретинит – требуется специфическая противовирусная терапия. Для лечения ЦМВ-инфекции у этих групп пациентов используются атипичные нуклеозиды (ганцикловир – Цимевен и валганцикловир – Вальцит), в сочетании со специфическим иммуноглобулином (Неоцитотект), а так же не зарегистрированные в РФ фоскарнет и цидофовир. Терапия ганцикловиром тяжело переносится пациентами, препарат высокотоксичен.
Остальные противовирусные препараты, широко используемые в России, не имеют доказательной базы и не могут быть рекомендованы.
Диагностика цитомегаловирусной инфекции сложна, и даже наличие положительных результатов анализов не всегда можно связать с имеющимся заболеванием, так как носительство ЦМВ после первичной инфекции пожизненное и вирус периодически определяется в секретах (слюна, моча и т.д.).
Вирус можно выявить методом ПЦР в крови, ликворе, слюне и других биологических жидкостях. Так же можно исследовать кровь на специфические антитела к вирусу (IgM, IgG) различными методами, но надо иметь ввиду, что широко распространенный метод иммуноферментного анализа (ИФА) не надежен и может часто давать ложноположительные результаты, поэтому нельзя диагностировать острую инфекцию на основании выявления в ИФА положительных IgM. Существуют референс-методы (ХЛИА, иммуноблот), которыми можно проверить результаты, полученные в ИФА, и только после этого решать вопрос о диагнозе.
У детей, рожденных от матерей, инфицированных ЦМВ до беременности в крови определяются положительные антитела класса IgG, которые могут сохраняться до года и более, что является носительством материнских антител и не является критерием инфекции.
Вирус герпеса 6 типа
Самое известное заболевание, вызываемое этим вирусом – внезапная экзантема (розеола).
Заболевание встречается чаще в возрасте около года ( от 6 месяцев до 2 лет) и характеризуется стойкой трехдневной лихорадкой без других симптомов, что чаще связывается с прорезыванием зубов. В некоторых случаях наблюдаются умеренные катаральные симптомы (насморк, подкашливание, иногда тонзиллит с налетами), почти у всех детей увеличены затылочные лимфатические узлы. На 4 сутки, после снижения температуры до нормальной, появляется типичная пятнисто-папулезная сыпь, которая сохраняется от нескольких часов до 2-3 дней. Сыпь может быть различной интенсивности. В этот период ребенок становится очень капризным, постоянно висит на руках у матери, отказывается от еды. В довольно большой части случаев заболевание может протекать без сыпи, только с лихорадкой. Осложнения очень редки, в основном – фебрильные судороги на фоне лихорадки.
Так же первичная инфекция может протекать в виде синдрома инфекционного мононуклеоза у более старших детей или респираторной инфекции. Иногда, очень редко, этот вирус вызывает энцефалиты. Как и для других герпес-вирусов, после перенесенной инфекции сохраняется пожизненное персистирование вируса в организме.
Диагноз можно подтвердить обнаружением вируса в крови или в других секретах методом ПЦР или ретроспективно по появлению специфических IgG после перенесенной первичной инфекции.
Важно знать, что после первичного инфицирования ВЭБ, ЦМВ, вирусом герпеса 6 типа персистирование вирусов в организме продолжается в течение всей жизни, антитела классов IgG будут определяться так же пожизненно в различных титрах, так же вирусы периодически могут определятся в различных жидкостях (моча, слюна, отделяемое с ротоглотки) организма методом ПЦР, что не является реактивацией вируса и в лечении не нуждается.
Реактивация вирусов происходит очень редко, в основном при развитии иммунодефицитного состояния, ассоциированного или с ВИЧ-инфекцией или с медикаментозной иммуносупрессией.
В настоящее время довольно модно в научных работах связывать персистирующие герпес-вирусные инфекции с довольно широким кругом соматических, аутоиммунных заболеваний, таких, как ревматоидный артрит, гломерулонефриты, воспалительные заболевания кишечника. В некоторых случаях, первичная герпес-вирусная инфекция, как и любая другая вирусная инфекция, может быть триггером, то есть пусковым моментом такого заболевания, но это не означает, что сама инфекция в данном случае нуждается в специфической противовирусной терапии.
Источник
Согласно данным ВОЗ, вирусом простого герпеса первого типа (ВПГ-1) во всем мире инфицировано около 3,7 млрд человек в возрасте до 50 лет, что составляет 67% населения.
Большинство населения заражается ВПГ-1 еще в детстве, после чего развивается его пожизненная персистенция в организме человека.
Частые рецидивы орального герпеса сопряжены з развитием психологического дискомфорта и множества социальных проблем. Герпетическая инфекция представляет особую опасность для пациентов, имеющих ослабленную иммунную систему, а также для новорожденных.
В этой статье на estet-portal.com читайте о современных принципах лечения орального герпеса, которые отвечают международным рекомендациям и постулатам доказательной медицины.
Почему необходимо проводить лечение рецидивов герпетической инфекции
Согласно современным научным представлениям, системна противовирусная терапия герпетической инфекции способствует сокращению продолжительности и снижению выраженности признаков обострения инфекции, тем самым повышая качество жизни пациентов.
Существуют сведения, что применение противовирусной терапии герпетической инфекции снижает риск передачи её другим лицам на 48%.
Следите за нашими новостями в Facebook
Известно, что ВПГ-1 может вызывать не только классический herpes labialis, но также и генитальный герпес.
Пациент больше всего заразен в период обострения инфекции – в это время необходимо исключить совместное пользование предметами, которые могут контактировать со слюной, а также ограничить поцелуи и орогенитальные сексуальные сношения.

Симптомы оральной герпетической инфекции у иммунокомпетентных пациентов
Инкубационный период составляет от 2 до 12 дней. Течение первичной инфекции, в большинстве случаев, асимптоматическое.
Иногда при первичной инфекции может наблюдаться лихорадка и фарингит – такие проявления герпеса часто остаются без внимания. Через несколько дней на слизистой оболочке ротовой области и глотки могут появиться характерные высыпания, которые сопровождаются болью и регионарной лимфаденопатией.
Рецидивы орального герпеса характеризуются стереотипной локализацией характерных высыпаний, которым могут предшествовать ощущение местного зуда, покалывания и жжения.
Как правило, везикулы и изъязвления располагаются вдоль красной каймы губ. Со временем повреждения покрываются корочкой и заживают на протяжении 10 дней.
Герпес, о котором Вы даже не догадывались
Лечение рецидива орального герпеса у иммунокомпетентных пациентов
Лечение рецидива орального герпеса должно проводиться всем пациентам и имеет важное значения для предупреждения развития неврологических симптомов инфекции.
Лечение рецидива герпетической инфекции должно быть начато на протяжении первых 72 часов после появления первых симптомов заболевания.
На сегодняшний день международные протоколы в качестве этиотропной терапии орального герпеса у иммунокомпетентных пациентов рекомендуют использовать такие препараты:
1. Ацикловир 200 мг 5 р/д;
2. Валацикловир 2 г 1 р/д ;
3. Фамцикловир 1,5 г 1 р/д;
Осторожно – генитальный герпес
Продолжительность лечения: 5 дней. Если оральный герпес сопровождается местным болевым синдромом, пациенту стоит рекомендовать местное применение лидокаина в виде 5% мази 2-3 р/д. Необходимо предупредить пациента о возможном риске развития аллергической реакции на лидокаин.

Целесообразность местной терапии орального герпеса: доказательная медицина
Согласно современным международным рекомендациям, в лечении оральной формы герпесвирусной инфекции на первое место выступает системная противовирусная терапия.
По результатам клинических исследований, противовирусные кремы обладают очень низкой эффективностью в сравнении в системной противовирусной терапией герпетической инфекции.
Крем, содержащий ацикловир, снижает продолжительность оральной герпетической инфекции всего на 0,5 дня.
Предпочтение использования местной терапии орального герпеса пациентами обусловлено, скорее, большей доступностью противовирусных кремов (отпускаются без рецепта во многих странах, в том числе и Великобритании), а также некой стереотипностью мышления населения. Но это не имеет ничего общего с медициной доказательной.
Спасибо, что Вы остаётесь с estet-portal.com. Читайте другие интересные статьи в разделе «Дерматология». Вас также может заинтересовать Неприятности и опасности из-за вируса простого герпеса
Источник
Роза Исмаиловна Ягудина, д. фарм. н., проф., зав. кафедрой организации лекарственного обеспечения и фармакоэкономики и зав. лабораторией фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Евгения Евгеньевна Аринина, к. м. н., ведущий научный сотрудник лаборатории фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Герпес (herpes simplex) — это хроническое персистирующее заболевание, характеризующееся высыпанием групп пузырьков (везикул) на коже и слизистых оболочках. Его возбудители принадлежат к семейству герпесвирусов (Herpesviridae), которое в свою очередь подразделяется на три подсемейства: α, β и γ. У человека наиболее часто встречаются нейротрофные нейроинвазивные вирусы простого герпеса (ВПГ) двух видов: ВПГ-1 и ВПГ-2, которые относятся к подсемейству α и поражают нервную систему и слизистые оболочки. Они очень эффективно обходят иммунную систему человека, чем можно объяснить длительный скрытый период болезни, позволяющий вирусу максимально распространиться в организме.
ВПГ внедряется в клетки эпителия (слизистой полости рта, глотки или половых органов), где происходит его размножение. Пораженные клетки гибнут, в очаг воспаления мигрируют лимфоциты и макрофаги, происходит выброс биологически активных веществ, повреждение капилляров и соединительной ткани. Затем вирус проникает в чувствительные нервные окончания и по центростремительным нервным волокнам — в паравертебральные ганглии. В ядрах нейронов происходит репликация вируса, цикл репродукции продолжается около 10 часов с образованием в клетке от 50 до 200 тысяч вирионов. При нормальном иммунном ответе через 2–4 недели после заражения происходит разрешение первичного заболевания и элиминация ВПГ из тканей и органов. Однако в паравертебральных ганглиях возбудитель в латентном состоянии сохраняется в течение всей жизни. В любой момент может начаться реактивация размножения ВПГ и его перемещение по нервным волокнам к месту первичного вхождения (воротам инфекции) с рецидивом специфического инфекционно-воспалительного процесса и возможной диссеминацией инфекции.
Причины возникновения и распространение вируса простого герпеса
ВПГ устойчив к действию низких температур: от –20 до –70 °С он сохраняет жизнеспособность 10 и более лет, также как и после лиофильного высушивания. Однако ВПГ не устойчив к нагреванию: при 50–52 °С инактивируется через 30 минут, а при 37 °С — в течение 10 часов. Быстрее всего вирус разрушается под действием ультрафиолетовых и рентгеновских лучей, этилового спирта, эфира и других органических растворителей, протеолитических ферментов. На поверхности кожи и на влажных предметах при комнатной температуре ВПГ сохраняет жизнеспособность в течение 1–4 часов.
Источник распространения вируса герпеса — больные и инфицированные люди. При активной (манифестной) форме он выделяется с кровью, мочой, слюной, другими биологическими жидкостями (содержимое везикул, слезы, менструальная кровь, вагинальное и цервикальное отделяемое, сперма). При латентной форме (вирусоносительстве) ВПГ выделяется таким же образом, но в меньших количествах. Носительство активного вируса чаще всего наблюдается в течение первых 12 месяцев с момента инфицирования. Но при иммунодефицитных состояниях продолжительность этого периода может увеличиваться.
От человека к человеку ВПГ передается разными путями:
- контактно-бытовым;
- половым;
- парентеральным;
- вертикальным (от матери к плоду);
- аэрозольным.
Контактно-бытовой, половой и парентеральный механизмы передачи объединяют в один, называемый «перкутанным».
Наиболее распространена передача ВПГ контактно-бытовым путем — через посуду, предметы личной гигиены, предметы быта, постельное белье, также возможно заражение при поцелуях. В зависимости от механизма передачи вируса выделяют несколько клинических форм этого заболевания. Так, к группе риска при половом и парентеральном способах передачи относятся люди, имеющие беспорядочные половые связи, употребляющие наркотические препараты.
Клиническая картина
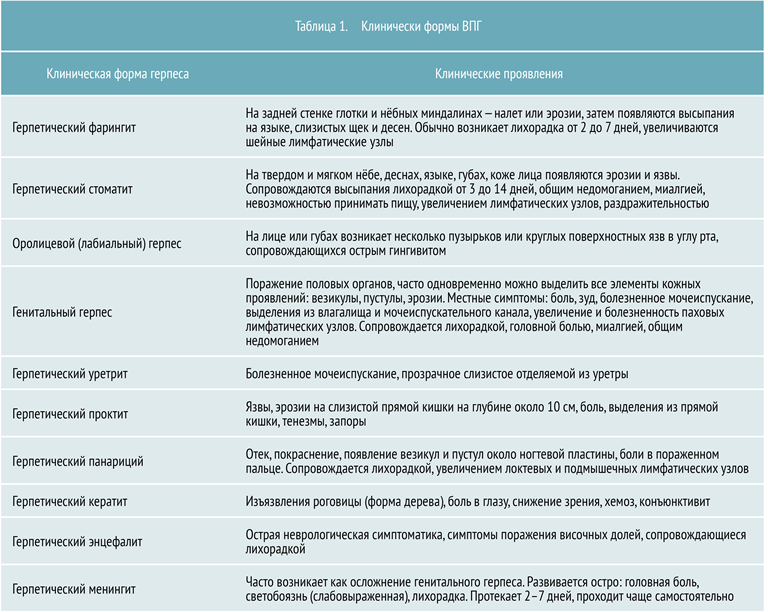
В зависимости от участков поражения выделяют несколько клинических форм ВПГ, представленных в таблице 1.
Первичный и вторичный герпес
Заболевание может протекать в следующих формах:
- Герпес первичный
- Герпес рецидивирующий
Первичный герпес чаще всего проявляется стоматитом или фарингитом, в основном у детей и молодых людей. Его инкубационный период составляет в среднем около недели. Общие признаки для всех клинических форм ВПГ: лихорадка, озноб, увеличение регионарных лимфоузлов.
У новорожденных ВПГ протекает в виде острого гингивостоматита, сопровождающегося эрозиями, язвами, некрозом на фоне отека и гиперемии слизистых оболочек.
Факторы риска при рецидивирующей форме герпеса: повышенное физическое или эмоциональное напряжения, общее истощение организма, различные виды лихорадки, травмы, гормональные изменения, поражение кожных покровов, хронические заболевания, переохлаждение, употребление алкоголя и наркотических препаратов, беспорядочная половая жизнь. При рецидиве вирус, находящийся в латентной стадии, активируется. В результате множество вирионов продвигаются по отросткам нейрона и переходят в эпителий кожи и слизистых оболочек. Рецидивирующий герпес развивается на фоне ограниченной гиперемии, с появлением пузырьков, содержащих прозрачный экссудат. Пузырьки обычно располагаются группами, в местах первичного поражения, там же обычно возникают жжение, покалывание и болезненность. Общее состояние человека при этом обычно не изменяется, но иногда может повышаться температура. Содержимое пузырьков может ссыхаться в корку, которая затем отпадает, или пузырьки вскрываются, образуя эрозию. В среднем рецидив герпеса клинически длится около 1–1,5 недели.
После первичного заражения ВПГ навсегда встраивается в геном клетки-хозяина и никогда не элиминируется иммунной системой.
ВПГ имеет циклическую активность (в течение 2–21 дня формируются пузырьки с вирусными частицами), периоды ремиссии, во время которых язвочки пропадают. Цикл репродукции вируса составляет 10 часов. Постепенно у человека формируется противовирусный иммунитет, и частота и тяжесть рецидивов уменьшается.
Формы и симптомы вируса герпеса 1 и 2 типа
Диагностика вируса герпеса: симптомы и лабораторные исследования
Диагностика ВПГ складывается из данных клинического осмотра и результатов лабораторных исследований, особенно значимых при латентной форме.
Оральный (лабиальный) герпес легко диагностируется лишь при наличии внешних проявлений — везикул, ран или язв. На ранних стадиях, когда симптомы заболевания отсутствуют, диагностировать герпес можно только лабораторными методами, который подтверждается при выделении вируса в культуре клеток и четырехкратном повышении титра антител при активной форме заболевания.
Для подтверждения диагноза и выбора терапии используется цитологический метод (в соскобах со дна везикул, окрашенных по Райту, Романовскому — Гимзе, видны характерные для герпеса гигантские клетки с внутриядерными включениями). Однако этот метод малочувствителен и не позволяет, например, отличить ВПГ от опоясывающего лишая.
Серологический метод с IgM и иммуноточечным гликопротеином G-специфичному HSV-тесту даёт более чем 98‑процентную специфичность и позволяет, таким образом, различить HSV-1 и HSV-2 типы герпеса.
Фармакотерапия: как вылечить герпес
В настоящее время существуют два основных направления в лечении вируса простого герпеса в организме человека:
- противовирусная терапия
- комплексная — иммунотерапия (специфическая + неспецифическая) + противовирусная
Противовирусная фармакотерапия
Ацикловир — противовирусный (противогерпетический) препарат, синтетический аналог нуклеозида тимидина, обладающий высокоизбирательным действием на вирусы герпеса. Внутри инфицированных клеток под действием вирусной тимидинкиназы проходит ряд последовательных реакций трансформации ацикловира в моно-, ди- и трифосфат ацикловира. Ацикловир трифосфат встраивается в цепочку вирусной ДНК и блокирует ее синтез посредством конкурентного ингибирования вирусной ДНК-полимеразы.
Специфичность и весьма высокая селективность действия также обусловлены его преимущественным накоплением в клетках, пораженных вирусом. Эффективен для большинства видов ВПГ, но лучший эффект достигается в лечении инфекций, вызванных herpes simplex типов 1 и 2, varicella zoster, слабее влияет на вирус Эпштейна — Барр и цитомегаловирусы.
После приема внутрь биологическая доступность ацикловира составляет 15–30 %, при этом создаются дозозависимые концентрации, достаточные для эффективного лечения вирусных заболеваний. Хорошо проникает во многие органы, ткани и жидкости организма, проникает через гематоэнцефалический и плацентарный барьеры, накапливается в грудном молоке. Связывание ацикловира с белками плазмы составляет 9–33 % и не зависит от его концентрации в плазме. Пища не оказывает значительного влияния на всасывание. Побочные реакции: тошнота, рвота, диарея, преходящее незначительное повышение активности ферментов печени, небольшое повышение концентрации мочевины и креатинина, гипербилирубинемия, головная боль, головокружение, анафилактические реакции, кожная сыпь, синдром Лайелла, синдром Стивенса — Джонсона, зуд, крапивница, сыпь, в том числе сенсибилизация. Таблетки и инъекционные формы ацикловира противопоказаны детям до 3‑х лет
Валацикловир — хлористоводородная соль L-валилового эфира ацикловира. Это пролекарство в организме абсорбируется из ЖКТ и при «первом прохождении» через кишечник и/или печень вследствие ферментативного гидролиза быстро и почти полностью (99 %) превращается в L-валин и ацикловир, который после фосфорилирования приобретает специфическую активность.
Побочные реакции: тошнота, рвота, гастралгия, снижение аппетита, повышение активности ACT, головокружение, головная боль, утомляемость, почечная недостаточность, микроангиопатия, гемолитическая анемия. Не зависит от приема пищи.
Пенцикловир — противовирусный препарат, активен в отношении вирусов herpes simplex 1 и 2 типа и varicella zoster. Пенцикловир попадает в инфицированные вирусом клетки, где под действием вирусной тимидинкиназы быстро превращается в монофосфат, который в свою очередь при участии клеточных ферментов переходит в трифосфат. Пенцикловира трифосфат находится в инфицированных вирусами клетках более 12 часов, подавляя в них синтез вирусной ДНК (дезоксирибонуклеиновой кислоты) и репликацию вирусов. Биодоступность пенцикловира — 77 %.
Побочные реакции: возможны жжение, пощипывание или онемение сразу же после нанесения препарата.
Фамцикловир — после приема внутрь фамцикловир быстро и почти полностью всасывается и превращается в активный пенцикловир.
Побочные реакции: головная боль, головокружение, повышение концентрации билирубина и активности «печеночных» трансаминаз, тошнота, рвота, диарея, боль в животе, кожная сыпь, зуд, повышенная потливость.
Ганцикловир — синтетический аналог 2′-дезоксигуанозина, который подавляет размножение вирусов герпеса. Активен в отношении цитомегаловируса человека (ЦМВ), вирусов простого герпеса 1‑го и 2‑го типа, вирусов герпеса человека 6, 7 и 8 типа, Эпштейна — Барр, ветряной оспы и гепатита В. В инфицированных клетках под действием вирусной протеинкиназы UL97 ганцикловир вначале фосфорилируется с образованием ганцикловира монофосфата, под действием клеточных киназ переходит в трифосфат, а затем подвергается медленному внутриклеточному метаболизму. Так как фосфорилирование ганцикловира в большой степени зависит от действия вирусной киназы, оно происходит преимущественно в инфицированных клетках. Рекомендуется принимать во время еды.
Валганцикловир — L-валиловый эфир (пролекарство) ганцикловира, после приема внутрь быстро превращающийся в ганцикловир под действием кишечных и печеночных эстераз. Рекомендуется принимать во время еды.
Все перечисленные выше препараты — средства «скорой помощи» при любых формах герпеса.
Иммунотерапия простого герпеса
Нарушение иммунного ответа — одно из важнейших звеньев в патогенезе простого герпеса, так как часто заболевание протекает на фоне подавления иммунных реакций. Происходит снижение общего количества Т- и В-клеток, изменение их функциональной активности, наблюдаются нарушения в макрофагальном звене иммунитета, в системе интерферона.
Неспецифическая иммунотерапия включает в себя использование:
- иммуноглобулина;
- интерферонов и индукторов интерферона;
- препаратов, стимулирующих Т- и В-звенья клеточного иммунитета и фагоцитоз.
Механизм действия иммуноглобулинов при герпесе длительное время объясняли заместительным эффектом на фоне присущей этому заболеванию несостоятельности гуморального иммунитета. В последние годы было установлено, что препараты иммуноглобулинов обладают также иммуномодулирующим и антитоксическим действием, активируют опсоно-фагоцитарные реакции.
Для лечения рецидивирующего герпеса применяют иммуноглобулин человеческий нормальный. Препарат содержит достаточное для достижения терапевтического эффекта количество специфических противогерпетических антител.
Интерферон (ИФ) — фактор естественного иммунитета, продуцируется клетками в ответ на воздействие вирусов, бактерий, чужеродных антигенов и активирует реакцию элиминации возбудителей инфекции. Помимо противовирусной активности интерферон обладает антипролиферативным и иммунорегулирующим действием. ИФ повышает неспецифическую резистентность клеток (стимулирует фагоцитоз, увеличивает активность естественных киллеров). Широкий спектр противовирусной активности, отсутствие резистентных к интерферону штаммов вирусов предопределили перспективу его использования как средства этиопатогенетической терапии простого герпеса.
Для лечения различных форм рецидивирующего герпеса используются рекомбинантный альфа-2а интерферон и созданный комбинированный препарат, который состоит из иммуноглобулинов и рекомбинантного альфа-2а интерферона в виде суппозиториев для ректального и вагинального введения.
С помощью препаратов интерферона (природных или генно-инженерных) осуществляется заместительная терапия, в результате чего может блокироваться продукция собственного эндогенного ИФ пациента. Это необходимо принимать во внимание при назначении длительных (более двух недель) курсов ИФ-терапии, особенно генно-инженерных форм. В случаях длительного назначения больным ИФ отменять их следует постепенно, снижая частоту приема до трех, далее двух раз в неделю с последующей полной отменой препарата.
Тилорон, тетрагидроксиглюкопиранозилксантен — индукторы ИФ, стимулируют выработку эндогенного ИФ в организме больного. Это объясняет терапевтический эффект перечисленных препаратов при многих вирусных заболеваниях (рецидивирующем герпесе, гриппе, аденовирусной инфекции), что позволяет рекомендовать их в комплексном лечении всех герпетических заболеваний, особенно у больных, страдающих частыми простудными заболеваниями и ОРВИ.
Специфическая иммунотерапия состоит в применении герпетической вакцины (поливалентной, тканевой, инактивированной). Лечебный эффект вакцины связан со стимуляцией специфических реакций противовирусного иммунитета, восстановлением функциональной активности иммунокомпетентных клеток и специфической десенсибилизацией организма.
Комплексное лечение вируса простого герпеса
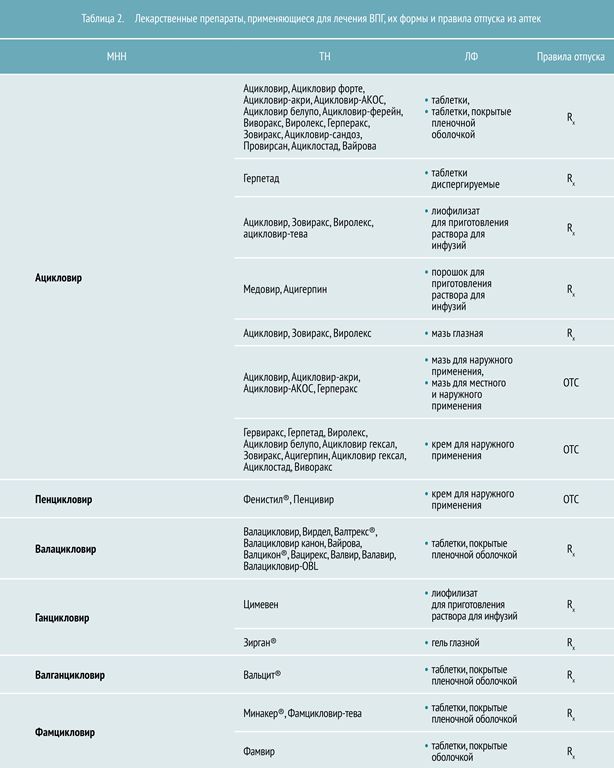
Учитывая патогенез, целесообразно использовать препараты с различным механизмом действия. Это препятствует появлению резистентных штаммов ВПГ, а применение интерферонов и их индукторов в сочетании с герпетической вакциной и иммуномодуляторами позволяет комплексно решать вопросы терапии. В таблице 2 представлены препараты, зарегистрированные на территории РФ для лечения ВПГ.Препараты при лечении вируса герпеса

Источник